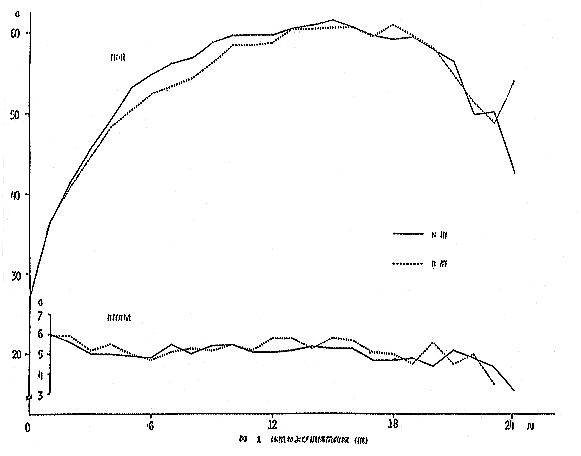
恾丂侾 懱廳偍傛傃愛塧検嬋慄乮梇乯
 |
丂兞慄徠幩僂僀儞僫乕僜乕僙乕僕偺埨慡惈傪挷傋傞栚揑偱丄儅僂僗偵傛傞俀係僇寧娫偺枬惈撆惈帋尡傪峴側偭偨偺偱丄偦偺寢壥偵偮偄偰曬崘偡傞丅
丂幚尡偵梡偄偨僂僀儞僫乕僜乕僙乕僕偼丄崅嶈僴儉惢偱丄擔杮尨巕椡尋媶強崅嶈尋媶強偵偍偄偰俇侽侽倠倰倎倓偺兞慄徠幩傪峴偭偨丅偦偺屻搥寢姡憞偟丄偙傟傪専懱偲偟偰俆倵乛倵亾偺妱偵僆儕僄儞僞儖峺曣惢儅僂僗帞堢梡屌宆帞椏乮俵俥乯偵揧壛偟偨丅
丂惷壀導幚尡摦暔擾嬈嫤摨慻崌嶻偺係廡椷丄帗梇偺倓倓倄宯儅僂僗乮俽俹俥乯傪峸擖屻侾廡娫撻壔帞堢偟丄俆廡楊帪偵寬峃偲巚傢傟傞儅僂僗傪丄帗梇奺乆侾孮俇侽旵偐傜側傞俀孮偵暘偗丄旕徠幩孮乮埲壓俶孮乯偍傛傃徠幩孮乮埲壓俼孮乯偲偟偨丅俶孮偵偼徠幩傪峴傢側偐偭偨僂僀儞僫乕僜乕僙乕僕傪揧壛偟偨屌宆帞椏傪丄俼孮偵偼徠幩偟偨僂僀儞僫乕僜乕僙乕僕傪揧壛偟偨屌宆帞椏傪偦傟偧傟帺桼偵愛庢偝偣偨丅
丂側偍丄摦暔偼摉強儅僂僗帞堢幒乮壏搙丗俀俁亇侾亷丄幖搙丗俆俆亇俆亾丄徠柧丗侾俀帪娫柧丄侾俀帪娫埫乯偵偰帞堢偟丄僾儔僗僠僢僋惢儅僂僗働乕僗侾屄偵偮偒俀旵偯偮廂梕偟偨丅堸悈偼帺摦媼悈憰抲偵傛傝悈摴悈傪帺桼偵愛庢偝偣偨丅
丂堦斒徢忬偍傛傃巰朣偺桳柍偼枅擔娤嶡偟丄幚尡奐巒屻俇儢寧栚傑偱偼廡侾夞丄侾俀僇寧栚傑偱妘廡丄偦傟埲崀俀係儢寧栚傑偱寧侾夞偺妱偱懱廳偍傛傃愛塧検傪應掕偟偨丅
丂幚尡奐巒屻侾俀儢寧栚偱奺孮俆旵丄俀係儢寧栚傑偱惗懚偡傞慡偰偺摦暔偵偮偄偰丄娽鈢惷柆憄傛傝嵦寣偟寣塼宍懺妛揑専嵏傪丄傑偨抐摢嵦寣偟暘棧偟偨寣惔傪梡偄偰寣惔惗壔妛揑専嵏傪峴側偭偨丅
丂寣塼宍懺妛揑専嵏偲偟偰偼丄敀寣媴悢乮倂俛俠乯丄愒寣媴悢乮俼俛俠乯丄僿儌僌儘價儞検乮俫倐乯丆僿儅僩僋儕僢僩抣乮俫倲乯丆暯嬒愒寣媴梕愊乮俵俠倁乯丄暯嬒愒寣媴寣怓慺検乮俵俠俫乯丆暯嬒愒寣媴寣怓慺擹搙乮俵俠俫俠乯丆寣彫斅梕愊斾乮俹們倲乯偍傛傃暯嬒寣彫斅梕愊乮俵俹倁乯偵偮偄偰俠倧倳倢倲倕倰丂俠倧倳値倲倕倰丂俵倧倓倕倢丂俽俹傪梡偄偰應掕偟丄偝傜偵揾枙昗杮乮僊儉僓愼怓乯傪嶌傝丄敀寣媴昐暘斾傪嶼弌偟偨丅
丂寣惔惗壔妛揑専嵏偱偼丄憤僞儞僷僋検乮俿亅俹俼俷丆榓岝僉僢僩乯丄傾儖僽儈儞検乮俙俴俛丆榓岝僉僢僩乯丄擜慺拏慺検乮俛倀俶丆僔僲僥僗僩乯丄寣摐抣乮俧俴倀丆俛俵倄僉僢僩乯丄僩儕僌儕僙儔僀僪乮俿亅俧俴倄丆俛俵倄僉僢僩乯丄傾儖僇儕惈儂僗僼傽僞乕僛乮俙俴俹丆榓岝僉僢僩乯丄僩儔儞僗傾儈僫乕僛乮俧俹俿丆塰尋僉僢僩乯丄偍傛傃擕巁扙悈慺峺慺乮俴俢俫丆僔僲僥僗僩乯傪俧倕倣倱倎倕們丂係宆僆乕僩傾僫儔僀僓乕偱丄偝傜偵僫僩儕僂儉乮俶倎乯偍傛傃僇儕僂儉乮俲乯傪擔棫揹夝幙帺摦暘愅婡俈侽俀宆偱應掕偟偨丅
丂傑偨侾俀偍傛傃俀係儢寧栚偵寣塼専嵏傪峴側偭偨摦暔偵偮偄偰丄昦棟夝朥傪峴側偄丄憻婍偺廳検應掕乮擼丄怱憻丄攛丄娞憻丄恡憻丄銪憻丄暃恡丄惛憙丄棏憙乯偍傛傃擏娽揑専嵏傪峴側偭偨屻丄侾侽亾拞惈儂儖儅儕儞塼偵屌掕偟丄忢朄偵廬偭偰僿儅僩僉僔儕儞亅僄僆僔儞愼怓昗杮傪嶌惢偟慻怐妛揑専嵏偵嫙偟偨丅専嵏偟偨憻婍偼丄忋婰偺懠偵壓悅懱丄峛忬態丄嫻態丄妠壓態丄鋁憻丄堓丄彫挵丄戝挵丄惛憙忋懱丄惛擷丄巕媨丄銷泖丄崪悜乮戝戁崪乯丄挵娫枌儕儞僷愡偍傛傃愐悜偱偁傞丅
丂搑拞巰朣摦暔偵偮偄偰傕昦棟夝朥傪峴側偄丄憻婍偺擏娽揑偍傛傃慻怐妛揑専嵏傪峴側偭偨丅
丂奺孮嫟偵丄俀係儢寧娫偵傢偨傝徠幩偵傛傞偲峫偊傜傟傞徢忬偺敪尰偼尒傜傟側偄丅
丂梇偱偼丄俆儢寧栚偐傜侾侽儢寧栚偵偐偗偰丄俼孮偵俶孮偲斾傋偰懱廳憹壛偺寉搙偺梷惂偑尒傜傟傞偑丄偦偺屻摿婰偡傋偒嵎偼尒傜傟側偄丅愛塧検偱偼丄係丄俉丄侾俀丄侾俁偍傛傃俀侽儢寧栚偱俶孮偵懳偟偰俼孮偱桳堄偺憹壛偁傞偄偼尭彮偑擣傔傜傟傞偑丄堦掕偺孹岦偼尒傜傟側偄丅丂帗偱偼丄侾侾儢寧栚埲屻俼孮偺懱廳偑俶孮傛傝崅抣傪帵偡偑丄俶孮偲偺娫偵桳堄嵎偼擣傔傜傟側偄丅愛塧検偱偼丄俀丄侾侽偍傛傃侾俀儢寧栚偱俼孮偵桳堄偺憹壛偁傞偄偼尭彮傪擣傔傞偑丄堦掕偺孹岦偼尒傜傟側偄丅
 |
 |
丂奺孮嫟偵丄幚尡奐巒屻俋儢寧栚傑偱嶶敪揑偵巰朣偑傒傜傟傞偑丄侾俀儢寧栚傛傝巰朣悢偺憹壛傪帵偡丅傑偨帗傛傝梇偵傗傗巰朣悢偑懡偔擣傔傜傟傞偑丄俶孮偲俼孮偺娫偵嵎偼尒傜傟側偄丅
丂僀乯侾俀儢寧栚丗梇偺敀寣媴悢偍傛傃敀寣媴昐暘斾偺暘梩妀岲拞媴丄儕儞僷媴偍傛傃扨媴偵桳堄偺曄壔偑尒傜傟傞偑丄帗偱偼嵎偼擣傔傜傟側偄丅
丂儘乯俀係儢寧栚丗梇偺俼孮偵偍偄偰丄愒寣媴悢丄俫倐丆俫倲偍傛傃扨媴偑俶孮偵斾傋桳堄側尭彮傪帵偡丅帗偱偼俫倲丆俵俠俫丆俵俠俫俠偵俶孮偵斾傋桳堄側尭彮偁傞偄偼憹壛傪擣傔傞丅
丂僀乯侾俀儢寧栚丗梇偺俼孮偱俶倎偑俶孮偵斾傋桳堄側尭彮傪帵偡偑丄帗偱偼嵎傪擣傔側偄丅
丂儘乯俀係儢寧栚丗梇偺俼孮偱寣摐抣偑俶孮偵斾傋桳堄側憹壛傪丄傑偨帗偱偼俶倎偑俼孮偱桳堄側尭彮傪帵偡丅
丂侾俀儢寧栚偱偼帗偺俼孮偱丄擼偺幚廳検偵桳堄偺憹壛傪擣傔傞偑丄懠偵偼斾廳検傪娷傔曄壔偼尒傜傟側偄丅
丂俀係儢寧栚偱偼梇偺俼孮偱暃恡偺斾廳検偑俶孮偵斾傋桳堄偺尭彮傪帵偡偑丄幚廳検偱偼嵎偼尒傜傟側偄丅
丂側偍丄幚廳検偲斾廳検偑嫟偵嵎傪帵偡憻婍偼椉帪婜傪捠偟偰擣傔傜傟側偄丅
丂侾俀儢寧栚丗奺孮偺庡側曄壔偼丄攛偍傛傃旂晢偵擣傔傜傟傞丅梇偱偼丄攛偺庮釒偑俶孮偱俁椺丄俼孮偱俀椺傒傜傟傞丅旂晢偺庮釒偑俶孮偵侾椺傒傜傟傞丅帗偱偼丄攛偺庮釃偑俶媦傃俼孮偵奺侾椺尒傜傟傞丅
丂俀係儢寧栚丗庮釒偺宍惉偼丄攛偵嵟傕懡偔丄梇偺俶孮偱俆椺丄俼孮偱係椺丄帗偺俶孮偱俀椺丄俼孮偱俇椺傒傜傟傞丅偦偺懠偺憻婍偱偼丄梇偺俶孮偺侾椺偵怱憻昞柺偺敀曄壔偑傒傜傟丄娞偱偼梇偺俶孮偺俁椺丄俼孮偺侾椺丄帗偱偼俶孮偺俁椺偵庮釒傪擣傔傞丅傑偨旂晢偱偼丄捵釃傪敽偆寢愡惈曄壔偑帗偺俶孮偍傛傃俼孮偵奺乆侾椺尒傜傟丄儕儞僷愡偺庮戝偑帗偺俶孮偱俁椺丄俼孮偱係椺偵傒傜傟傞丅
丂搑拞巰朣摦暔乮昞俈乯丗搑拞巰朣摦暔偵擣傔傜傟偨曄壔偺庡側傕偺傪昞偵帵偟偨丅偙傟傜偺偆偪嵟傕敪惗昿搙偺崅偄傕偺偼攛偺庮釒偱梇偺俶孮偱偼俁侾乛係俋椺丄俼孮偱偼俁俈乛俆侾椺丄帗偺俶孮俀俆乛係俉椺丄俼孮俀係乛係係椺偱偁偭偨丅偙傟傜偺寢愡偼偄偢傟傕擕敀怓偺峝搙姶傪桳偡傞傕偺偱偁傞丅
丂銪憻偍傛傃儕儞僷愡偺庮戝偑丄攛偺庮釒偵師偄偱懡偔尒傜傟傞丅傑偨旂壓偺庮釒偑梇偱偼俶孮俁椺丄俼孮俀椺偵擣傔傜傟傞偺偵懳偟偰丄帗偱偼俶孮侾俁椺丄俼孮侾係椺偲帗偵懡偔尒傜傟傞丅偙傟傜偺寢愡偼丄擕敀怓挷偱攳棧惈偑傛偔丄傑偨偙傟傜偺寢愡偺拞偵偼擷朎傪宍惉偡傞傕偺傕偁傞丅
丂娞憻丄恡憻丄惛憙丄棏憙偍傛傃巕媨偱彮悢椺偵寢愡偁傞偄偼寣庮偍傛傃擷朎偺宍惉偑擣傔傜傟傞丅
丂侾俀儢寧栚乮昞俉乯丗攛偺態庮傪梇偺俶孮偱俁椺丄俼孮偱俀椺丄傑偨帗偱偼俶孮偍傛傃俼孮偱奺侾椺擣傔傞丅偦偺懠梇偺俶孮偺侾椺偵旂晢偺擕摢庮傪擣傔傞丅庮釃敪尰摦暔悢偼梇偺俶孮偱俁乛俆椺乮俇侽丏侽亾乯丄俼孮俀乛俆椺乮係侽丏侽亾乯丄傑偨帗偱偼俶孮偍傛傃俼孮嫟偵侾乛俆椺乮俀侽亾乯偱偁傞丅
丂俀係儢寧栚乮昞俋乯丗梇丄帗嫟偵奺孮攛偺態庮偑懡偄丅傑偨梇丄帗嫟偵俶孮偱娞憻偺寢愡惈憹怋傪擣傔傞丅偦偺懠偵怱憻丄暃恡丄擕態側偳偺庮釒偁傞偄偼敀寣昦傪嶶尒偡傞丅庮釃敪尰摦暔悢偼丄梇偺俶孮俇乛俇椺乮侾侽侽亾乯丄俼孮係乛係椺乮侾侽侽亾乯丄傑偨帗偺俶孮偼係乛俈椺乮俆俈丏侾亾乯丄俼孮俉乛侾侾椺乮俈俀丏俈亾乯偱丄梇丄帗偄偢傟傕孮娫偵嵎傪擣傔側偄丅
丂搑拞巰朣摦暔乮昞侾侽丄昞侾侾乯丗梇丄帗嫟偵攛偺態庮偍傛傃敀寣昦偑丄梇偱偼娞憻偺寢愡惈憹怋偑丄傑偨帗偱偼擕態庮釃偺敪惗偑懡悢擣傔傜傟傞丅偦偺懠偺庮釃偺敪惗晹埵偼丄梇偱恡憻丄銪憻丄鋁憻丄惛憙丄慜棫態丄儕儞僷愡丄旂壓慻怐偍傛傃彫挵丄傑偨帗偱偼娞憻丄棏憙丄暃恡丄儕儞僷愡丄旂晢偍傛傃旂壓慻怐側偳偱偁傞偑丄偄偢傟傕嶶敪揑偱偁傞丅偙傟傜偺庮釃偺敪尰悢偼丄梇丄帗嫟偵孮娫偵桳堄嵎傪擣傔側偄丅
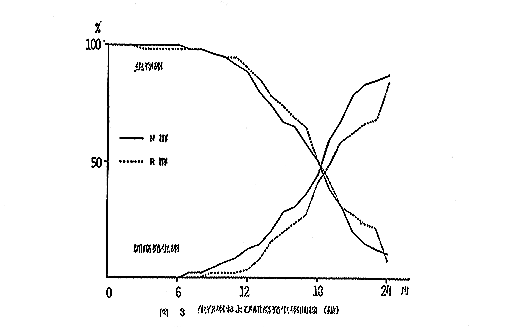
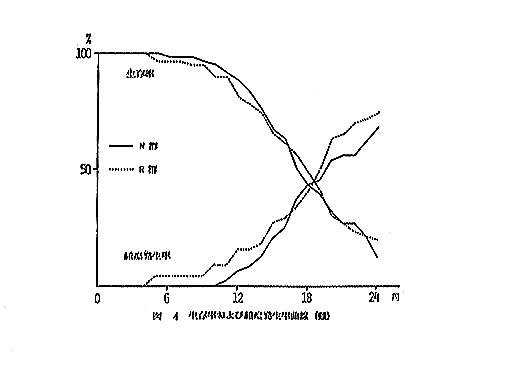
丂搑拞巰朣摦暔偺庮釃敪尰帪婜偼戞俁恾偍傛傃戞係恾偵帵偡傛偆偵丄梇偱偼俶孮偱俈儢寧栚丄俼孮偱俋儢寧栚偱偁偭偨丅傑偨帗偱偼俶孮偱侾侾儢寧栚丄俼孮偱俆儢寧栚偱偁偭偨丅
丂庮釃敪尰摦暔悢偼丄梇偱偼俶孮偱係俁乛係俋椺乮俉俈丏俉亾乯丄俼孮偱係俁乛俆侾椺乮俉係丏俁亾乯丄傑偨帗偱偼俶孮俁俁乛係俉椺乮俇俉丏俉亾乯丄俼孮俁俁乛係係椺乮俈俆丏侽亾乯偱丄梇丄帗嫟偵孮娫偵嵎偼擣傔傜傟側偄丅
 |
 |
丂兞慄徠幩僂僀儞僫乕僜乕僙乕僕偺埨慡惈傪挷傋傞栚揑偱儅僂僗偵傛傞俀係儢寧娫偺枬惈撆惈帋尡傪峴側偭偨丅
丂侾丏堦斒徢忬丄懱廳丄愛塧検偍傛傃巰朣棪偱偼俀係儢寧娫偵傢偨偭偰俶孮偲俼孮偲偺娫偵柧傜偐側嵎偼擣傔傜傟側偐偭偨丅
丂俀丏侾俀儢寧栚偍傛傃俀係儢寧栚偺寣塼宍懺妛揑専嵏偍傛傃寣惔惗壔妛揑専嵏偱偼丄俀係儢寧栚偱丄梇偺俼孮偺愒寣媴悢丄俫倐偍傛傃俫倲偑俶孮偵斾傋桳堄偺尭彮傪帵偡偑丄偙傟偼俶孮偺悢抣偑憹壛偟偨偨傔偱丄俼孮偺悢抣偼惓忢斖埻撪偲峫偊傜傟傞丅偟偐偟偙傟埲奜偵庒姳偺嵎偑擣傔傜傟偨偑丄柧傜偐側孹岦偑擣傔傜傟偢丄撆惈忋堄枴偺偁傞曄壔偲偼巚傢傟側偄丅
丂俁丏侾俀儢寧栚偍傛傃俀係儢寧栚偺昦棟妛揑専嵏偱偼丄偦偺憻婍廳検偍傛傃庮釃敪尰悢乮棪乯偵偼丄梇丄帗嫟偵孮娫偵嵎偼擣傔傜傟側偐偭偨丅摨條偵搑拞巰朣摦暔偺専嵏寢壥偱傕庮釃敪尰悢偵嵎偼擣傔傜傟側偐偭偨丅
丂埲忋偺偙偲偐傜丄兞慄徠幩僂僀儞僫乕僜乕僙乕僕傪儅僂僗偵搳梌偟偰傕丄徠幩偵傛傞偲峫偊傜傟傞塭嬁偼側偄傕偺偲峫偊傜傟傞丅
丂兞慄徠幩僂僀儞僫乕僜乕僙乕僕偺埨慡惈傪挷傋傞栚揑偱丄儔僢僩偵傛傞俀係儢寧娫偺枬惈撆惈帋尡傪峴偭偨偺偱丄偦偺寢壥偵偮偄偰曬崘偡傞丅
丂壢妛媄弍挕怘昳徠幩尋媶塣塩夛媍巜掕偺崅嶈僴儉惢僂僀儞僫乕僜乕僙乕僕傪昁梫偵墳偠偰嶌惢偟丄偙傟傪擇暘偟偰丄堦曽傪旕徠幩僂僀儞僫乕僜乕僙乕僕偲偟丄懠曽傪擔杮尨巕椡尋媶強崅嶈尋媶強偵偍偄偰俇侽侽倠倰倎倓偺兞慄徠幩傪峴偄徠幩僂僀儞僫乕僜乕僙乕僕偲偟丄偙傟傜傪敄曅忬偵愗抐偟搥寢姡憞偟偨丅偙偺帪偺曕巭傑傝偼俁俈丏俆亾偱偁偭偨丅偙偺姡憞僂僀儞僫乕僜乕僙乕僕傪暡嵱偟丄儔僢僩梡暡枛帞椏乮僆儕僄儞僞儖峺曣惢丄俵俥乯偵俀倂乛倂亾媦傃俆倂乛倂亾偺妱崌偵崿崌偟丄墌拰宆儁儗僢僩偵惉宆偟偰専懱帞椏偲偟偨丅偙傟傜偺帞椏傪俀係儢寧娫偵榡傝帺桼偵摦暔偵梌偊偨丅
丂惷壀導幚尡摦暔擾嬈嫤摨慻崌嶻偺惗屻係廡椷偺梇帗偺僂傿僗僞乕宯儔僢僩傪峸擖屻侾廡娫撻壔帞堢偟丄俆廡椷帪偵寬峃偲巚傢傟傞儔僢僩傪丄梇帗奺乆侾孮俁侽旵偐傜側傞係孮偵暘偗丄旕徠幩孮乮俀亾丗俶亅俀丆俆亾丗俶亅俆乯媦傃徠幩孮乮俀亾丗俼亅俀丆俆亾丗俼亅俆乯偲偟偨丅
丂側偍丄摦暔偼摉強儔僢僩帞堢幒乮壏搙丗俀俆亇侾亷丄幖搙俆俆亇俆亾丄徠柧丗侾俀帪娫柧丄侾俀帪娫埫丄侾侽侽亾怴慛嬻婥挷榓乯偵偰奺乆屄暿働乕僕偱帞堢偟丄堸悈偼帺摦媼悈憰抲偵傛傝悈摴悈傪帺桼偵愛庢偝偣偨丅
丂堦斒徢忬媦傃巰朣偺桳柍偵偮偄偰偼枅擔娤嶡偟丄懱廳媦傃愛塧検偼幚尡奐巒屻俁儢寧栚傑偱偼廡侾夞丄侾俀儢寧栚傑偱偼妘廡丄侾俉儢寧栚傑偱偼俁廡偵侾夞丄偦傟埲崀俀係儢寧栚傑偱寧侾夞偺妱崌偱應掕偟偨丅
丂幚尡奐巒屻俇丄侾俀媦傃侾俉儢寧栚偵奺孮俆旵丄俀係儢寧栚偵惗懚偡傞慡摦暔偵偮偄偰丄旜惷柆傛傝嵦寣偟寣塼宍懺妛専嵏傪丄傑偨抐摢嵦寣偟暘棧偟偨寣惔傪梡偄偰寣惔惗壔妛揑専嵏傪峴偄丄峏偵昦棟慻怐妛揑専嵏傪幚巤偟偨丅
丂搑拞帺慠巰朣偟偨摦暔偼敪尒屻壜媦揑懍傗偐偵夝朥偟丄擏娽強尒傪婰榐偟偨屻慻怐妛揑専嵏偵嫙偟偨丅側偍丄巰朣棪偺寁嶼偼倢倝倖倕亅倲倎倐倢倕丂倲倕們倛値倝倯倳倕傪梡偄偰峴偭偨丅
丂傑偨丄忋婰偺奺帪婜偵峴偭偨寣塼偺宍懺妛揑媦傃惗壔妛揑専嵏偲昦棟妛揑専嵏偺撪梕偼師偺捠傝偱偁傞丅
丂寣塼宍懺妛揑専嵏
丂丂愒寣媴媦傃敀寣媴悢乮俼俛俠丆倂俛俠乯丗僩乕傾儈僋儘僙儖
丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂僇僂儞僞乕
丂丂僿儌僌儘價儞検乮俫倐乯丗僔傾儞儊僩僿儌僌儘價儞朄
丂丂僿儅僩僋儕僢僩抣乮俫倲乯丗栄嵶娗墦怱朄
丂丂敀寣媴憸乮昐暘斾乯丗揾枙昗杮
丂寣惔惗壔妛揑専嵏
丂丂憤抈敀検乮俹倰倧倲倕倝値乯丗僺儏儗僢僩朄
丂丂傾儖僽儈儞乮俙倢倐倳倣倝値乯丗俫俙俛俠怓慺寢崌朄
丂丂僐儗僗僥儘乕儖乮俿亅俠倛倧倢丏丆俥亅俠倛倧倢丏乯丗倅倎倠偺
丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂曄朄
丂丂傾儖僇儕惈儂僗僼傽僞乕僛乮俙俴俹乯丗俲倝値倓丂倎値倓
丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂俲倝値倗朄
丂丂僩儔儞僗傾儈僫乕僛乮俧俷俿丆俧俹俿乯丗俼倕倝倲倣倎値亅
丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂俥倰倎値倠倕倢朄
丂丂擜慺拏慺乮倀亅俶乯丗埞栰丒婽壀偺僕傾僠儖儌僲僆僉僔儉
丂丂丂丂丂丂丂丂丂丂丂丂捈愙斾怓朄
丂丂梀棧帀朾巁乮俶俤俥俙乯丗僷僜僐僾儘僀儞斾怓朄
丂丂僩儕僌儕僙儔僀僪乮俿倰倝倗倷們倕倰倝倓倕乯丗俥倢倕倲倕倛倕倰
丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂偺曽朄
丂丂柍婡儕儞乮俽亅俹倝乯丗僒僼儔僯儞朄
丂丂憻婍廳検偺應掕丗擼丄壓悅懱丄峛忬態丄怱憻丄攛丄娞憻丄
丂丂丂丂丂丂丂丂丂丂恡憻丄暃恡丄銪憻丄惛憙媦傃棏憙
丂昦棟妛揑専嵏
丂丂擏娽揑専嵏丗懱昞柺偺宍忬媦傃憻婍丒慻怐偺擏娽揑専嵏
丂丂慻怐妛揑専嵏丗忋婰偺彅憻婍偺傎偐偵堓丄彫挵丄鋁憻丄崪悜丄
丂丂丂丂丂丂丂丂丂媦傃挵娫枌儕儞僷愡偺岝妛尠旝嬀偵傛傞専嵏
丂幚尡寢壥偺摑寁揑桳堄惈偼丄俽倲倳倓倕値倲乫倱丂倲亅倲倕倱倲偵傛傝摨堦揧壛検偺旕徠幩孮偲徠幩孮偺孮娫偱専摙偟偨丅
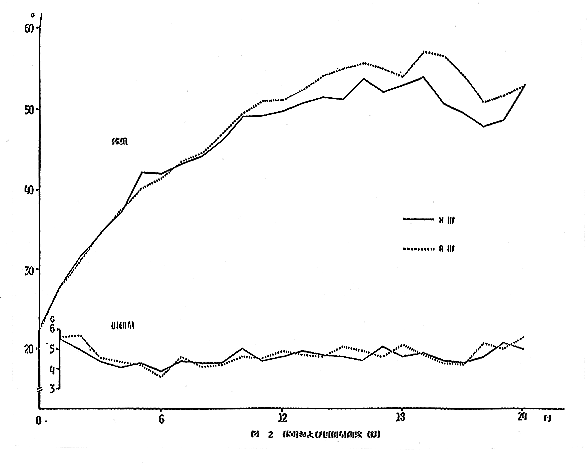
丂俀係儢寧傑偱偺帞堢慡婜娫傪捠偠偰丄梇帗奺孮偲傕偵摿婰偡傋偒徢忬偺敪尰傪尒側偄丅
丂梇帗偲傕偵幚尡奐巒屻俈侽廡栚崰傑偱杦傫偳嵎傪擣傔側偄偑丄偦偺屻梇偱偼俼亅俆孮偑俉侽廡栚偐傜俋侽廡栚偵偐偗偰堦帪揑偵懱廳憹壛偺梷惂媦傃憹壛傪帵偡丅帗偱偼丄俶亅俆孮偑俈侽廡栚埲崀俼亅俆孮偵斾傋憹壛偺孹岦傪帵偡丅
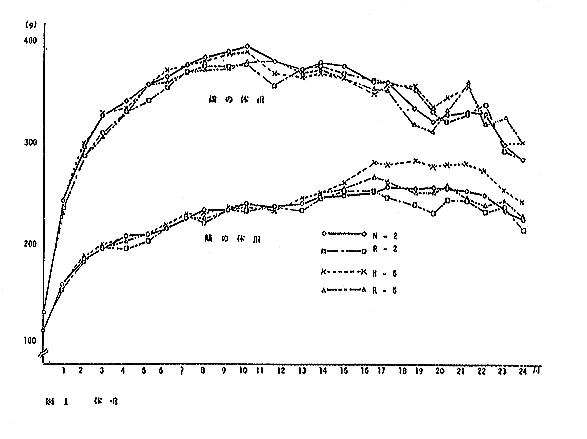 |
丂梇帗偲傕偵慡婜娫傪捠偠偰丄孮娫偵杦傫偳嵎傪尒側偄丅
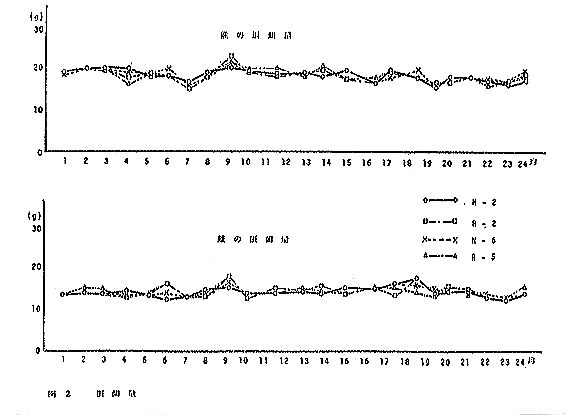 |
丂梇偱偼丄俼亅俀孮偑俶亅俀孮偵斾傋傗傗崅抣傪帵偟丄俼亅俆孮偑俶亅俆孮偵斾傋媡偵傗傗掅抣傪帵偡偑丄偄偢傟傕桳堄嵎傪尒側偄丅帗偱偼丄俼亅俀孮偑俶亅俀孮偵斾傋傗傗崅抣傪帵偡偑桳堄嵎傪尒側偄丅傑偨丄俼亅俆孮媦傃俶亅俆孮偺孮娫偵杦傫偳嵎傪擣傔側偄丅
丂俇儢寧栚乮昞俀乯丗梇偱偼丄俼亅俀孮偱俫倲抣偑俶亅俀孮偵斾傋丄傑偨丄帗偱偼丄俼亅俆孮偱俫倲抣偑俶亅俆孮偵斾傋丄偄偢傟傕桳堄偺尭彮傪帵偡丅
丂侾俀儢寧栚乮昞俀乯丗梇偱偼丄俼亅俆孮偱俼俛俠偑俶亅俆孮偵斾傋桳堄偺尭彮傪帵偟丄倂俛俠偑尭彮偺孹岦傪帵偡偑桳堄嵎傪尒側偄丅帗偱偼丄俼亅俀孮偱俫倲抣偑俶亅俀孮偵斾傋桳堄偺憹壛傪帵偡丅
丂侾俉儢寧栚乮昞俁乯丗梇偱偼丄俼亅俆孮偺俫倲抣偑俶亅俆孮偵斾傋桳堄偺尭彮傪帵偡奜偼丄奺崁栚偱孮娫偵杦傫偳嵎傪尒側偄丅傑偨帗偵偮偄偰傕杦傫偳孮娫偵嵎傪擣傔側偄丅
丂俀係儢寧栚乮昞俁乯丗梇帗偲傕偵孮娫偵嵎傪擣傔側偄丅
丂忋弎偺傛偆偵丄俇丄侾俀丄侾俉媦傃俀係儢寧栚偺奺帪婜偵偍偄偰丄敀寣媴昐暘斾傪娷傔摨堦揧壛検偺旕徠幩孮媦傃徠幩孮偺孮娫偵堦掕偺孹岦傪尒側偄丅
丂俇儢寧栚乮昞俆乯丗梇偱偼丄俼亅俀孮偱俠倛倧倢丏亾偑俶亅俀孮偵斾傋偰桳堄偺憹壛傪帵偟丄俧俷俿偑桳堄偺尭彮傪帵偡丅帗偱偼丄俼亅俀孮偱俽亅俹倝偑俶亅俀孮偵斾傋桳堄偺憹壛傪帵偡偑丄懠偺崁栚偱偼杦傫偳孮娫偵嵎傪尒側偄丅
丂侾俀儢寧栚乮昞俆乯丗梇偱偼孮娫偵杦傫偳嵎傪尒側偄丅帗偱偼丄俼亅俀孮偱俥亅俠倛倧倢丏偑俶亅俀孮偵斾傋桳堄偺尭彮傪帵偟丄俠倛倧倢丏亾偑桳堄偺憹壛傪帵偡丅
丂侾俉儢寧栚乮昞俇乯丗梇偱偼丄俼亅俀孮偱倀亅俶偑俶亅俀孮偵斾傋桳堄偺憹壛傪丄傑偨丄俼亅俆孮偱俙倢倐倳倣倝値偑俶亅俆孮偵斾傋桳堄偺憹壛傪丄倀亅俶偑媡偵桳堄偺尭彮傪帵偡丅帗偱偼丄俼亅俀孮偱俹倰倧倲倕倝値偑俶亅俀孮偵斾傋桳堄偺尭彮傪帵偟丄俽亅俹倝偑桳堄偺憹壛傪帵偡丅
丂傑偨俼亅俆孮偱俙倢倐倳倣倝値丆俧俹俿媦傃俿倰倝倗倢倷們倕倰倝倓倕偑偄偢傟偺俶亅俆孮偵斾傋偰桳堄偺尭彮傪帵偡丅
丂俀係儢寧栚乮昞俇乯丗梇偱偼孮娫偱杦傫偳嵎傪尒側偄丅帗偱偼丄俼亅俆孮偱俶俤俥俙偑俶亅俆孮偵斾傋桳堄偺尭彮傪帵偡奜偼杦傫偳嵎傪擣傔側偄丅
丂忋弎偺傛偆偵俇丄侾俀丄侾俉媦傃俀係儢寧栚偺奺帪婜偱孮娫偵偄偔偮偐偺嵎傪尒傞偑丄摨堦揧壛検偺旕徠幩孮媦傃徠幩孮偺孮娫偱堦掕偺孹岦傪尒側偄丅
丂俇丄侾俀丄侾俉媦傃俀係儢寧栚偺奺帪婜偵夝朥偟偨摦暔偺憻婍幚應抣媦傃懱廳斾偑偲傕偵摨堦曽岦偵嵎傪帵偡傕偺偵偮偄偰弎傋傞丅
丂俇儢寧栚乮昞俈乯丗梇偱偼丄俼亅俀孮偱怱憻偑俶亅俀孮偵斾傋桳堄偺尭彮傪帵偡丅帗偱偼丄俼亅俆孮偱擼偑俶亅俆孮偵斾傋憹壛偺孹岦傪帵偡丅
丂侾俀儢寧栚乮昞俉乯丗梇偱偼偲傕偵摨堦曽岦偵嵎傪帵偡憻婍傪尒側偄丅帗偱偼俼亅俆孮偱暃恡偑俶亅俆孮偱暃恡偑俶亅俆孮偵斾傋尭彮偺孹岦傪帵偡丅
丂侾俉儢寧栚乮昞俋乯丗梇偱偼丄俼亅俀孮偱擼媦傃暃恡偑俶亅俀孮偵斾傋偄偢傟傕尭彮偺孹岦傪丄攛偑憹壛偺孹岦傪帵偡丅帗偱偼丄俼亅俀孮偱擼偑俶亅俀孮偵斾傋尭彮偺孹岦傪帵偟丄俼亅俆孮偱壓悅懱丄峛忬態媦傃暃恡偑俶亅俆孮偵斾傋偄偢傟傕桳堄偺憹壛側偄偟偦偺孹岦傪帵偡丅
丂俀係儢寧栚乮昞侾侽乯丗梇偱偼丄俼亅俀孮偱暃恡丄銪憻媦傃惛憙偑俶亅俀孮偵斾傋偄偢傟傕尭彮偺孹岦傪帵偡丅帗偼偲傕偵摨堦曽岦偵嵎傪帵偡憻婍傪尒側偄丅
丂忋弎偺傛偆偵丄俇丄侾俀丄侾俉媦傃俀係儢寧栚偺奺帪婜偱偄偔偮偐偺嵎傪尒傞偑丄摨堦揧壛検偺旕徠幩孮媦傃徠幩孮偺孮娫偱堦掕偺孹岦傪擣傔側偄丅
丂俇儢寧栚丗梇帗偲傕偵奺孮偱曄壔傪擣傔側偄丅
丂侾俀儢寧栚丗梇偱偼庡側曄壔偲偟偰攛墛偑奺孮偱侾乣係椺擣傔傜傟傞奜丄俶亅俆孮偱攛偲嫻枌偺桙拝偑俀椺擣傔傜傟傞丅帗偱偼俶亅俀孮傪彍偔奺孮偱攛偲嫻枌偺桙拝偑侾乣俁椺擣傔傜傟傞丅
丂侾俉儢寧栚丗梇偱偼丄攛墛偑杦傫偳偺摦暔偵擣傔傜傟傞奜丄攛擽釃偁傞偄偼攛偲嫻枌偺桙拝偑暲懚偡傞摦暔傕彮悢椺擣傔傜傟傞丅傑偨恡憻偱偼昞柺偺慹偧偆壔偑奺孮侾乣俁椺擣傔傜傟傞丅惛憙偱偼曅懁惈偺堔弅偁傞偄偼敀怓庮釃偑丄奺孮偺杦傫偳偺摦暔偵傒傜傟傞丅帗偱偼丄攛墛傪奺孮偵俀乣俁椺丄傑偨攛擽釃偺暲懚偡傞傕偺偑奺孮偵侾乣俀椺擣傔傜傟傞丅偦偺奜丄娞憻偺戅怓丄恡憻偺昞柺慹偧偆壔丄巕媨拁擽媦傃棏憙偺擷庮宍惉乮棏憙幚幙偲曪枌偺娫偵燋塼條暔挋棷乯側偳偺曄壔傪嶶敪揑偵擣傔傞丅
丂俀係儢寧栚丗梇偱偼丄攛墛偑俶亅俀孮媦傃俼亅俀孮偱擣傔傜傟傞奜丄恡憻偱昞柺偺慹偧偆壔丄惛憙偺敀怓庮釃偑奺孮偺杦傫偳偺摦暔偵尒傜傟傞丅帗偱偼丄攛墛媦傃攛擽釃宍惉偑俶亅俀孮媦傃俼亅俆孮偱傒傜傟傞奜丄恡憻偱昞柺偺慹偧偆壔傪擣傔傞丅
丂傑偨丄娞憻偺弪怓媦傃旍戝丄銪憻偺庮戝丄巕媨拁擽丄壓悅懱寣庮丄棏憙偺擷庮宍惉媦傃旂壓慻怐偺庮釒宍惉側偳偺曄壔傪嶶敪揑偵擣傔傞丅
丂帺慠巰摦暔偺朥専強尒丗帞堢婜娫拞偵帺慠巰偟偨摦暔偺朥専強尒偼丄梇帗偲傕偵庡側曄壔偲偟偰攛偺擽釃媦傃廩偆偭寣偑奺孮偱偦傟偧傟俀乣俉椺傪擣傔傞丅
丂忋弎偺傛偆偵俇丄侾俀丄侾俉媦傃俀係儢寧栚偺掕婜夝朥媦傃帺慠巰夝朥椺偺擏娽揑強尒偵偼丄梇帗偲傕偵旕徠幩孮偲徠幩孮偺孮娫偵挊偟偄嵎偼擣傔傜傟側偄丅
丂俇丄侾俀丄侾俉媦傃俀係儢寧栚偺掕婜夝朥媦傃帺慠巰夝朥偟偨慻怐妛揑専嵏偺寢壥丄庮釃偵偮偄偰偼庮釃偺崁偱弎傋傞丅
丂俇儢寧栚乮昞侾侾乯丗庡側曄壔偲偟偰偼梇帗偲傕偵攛偱攛朎暻偺旍岤丄娞憻偱僌儕僜儞忊撪墌宍嵶朎怹弫丄惎嵶朎偺旍戝丄恡憻偱嵶擜娗撪忋旂惈墌拰偺弌尰傪尒傞丅偟偐偟丄偙傟傜偺曄壔偼旕徠幩孮偲徠幩孮偺孮娫偵嵎傪尒側偄丅
丂侾俀儢寧栚乮昞侾俀乯丗庡側曄壔偼梇帗偲傕偵攛偱攛朎暻旍岤丄恡憻偱嵶擜娗撪忋旂惈墌拰偁傞偄偼徤巕條墌拰側偳偱偁傞丅偙傟傜偺曄壔偼孮娫偵傎偲傫偳嵎傪尒側偄丅
丂侾俉儢寧栚乮昞侾俁乯丗梇帗偺庡側曄壔偼娞憻偱僌儕僜儞忊撪墌宍嵶朎怹弫丄恡憻偱枬惈偺巺媴懱婎掙枌旍岤丄擜嵶娗撪忋旂惈墌拰丄徤巕條墌拰丄擜嵶娗偺奼挘丄徤巕揌曄惈媦傃娫幙偺憹怋側偳丄偄傢備傞枬惈恡徢偺憸傪擣傔傞丅偦偺奜丄惛憙偱偼娫幙嵶朎偺憹怋傪擣傔傞丅偙傟傜偺曄壔偵偼孮娫偵嵎傪尒側偄丅
丂俀係儢寧栚乮昞侾係乯丗梇帗偲傕偵峛忬態丄怱憻丄攛丄娞憻丄恡憻丄銪憻丄暃恡媦傃惗怋婍乮惛憙丒棏憙乯側偳偵曄壔偑尒傜傟傞丅偦傟傜偺庡側曄壔偲偟偰偼丄攛偱攛朎暻旍岤丄婥娗巟攛墛側偳丄偄傢備傞攛墛憸傪掓偡傞傕偺傪懡偔擣傔傞丅恡憻偱偼枬惈偺巺媴懱偺婎掙枌旍岤丄擜嵶娗撪偺忋旂惈墌拰丄徤巕條墌拰丄擜嵶娗奼挘丄娫幙偺憹怋媦傃墌宍嵶朎偺怹弫側偳丄偄傢備傞枬惈恡徢偺憸傪掓偡傞傕偺傪尒傞丅偙傟傜偺曄壔偼梇帗偲傕偵孮娫偵堦掕偺孹岦傪尒側偄丅
丂傑偨丄偙偺奜偺憻婍偵偍偗傞曄壔偼嶶敪揑偱偁傝丄孮娫偵嵎傪尒側偄丅
丂忋弎偺傛偆偵俇丄侾俀丄侾俉媦傃俀係儢寧栚偺奺帪婜偱偺慻怐妛揑専嵏偺寢壥丄奺帪婜偺梇帗偲偲傕偵曄壔傪傕偭偨摦暔悢媦傃曄壔偺撪梕偵傕丄旕徠幩孮偲徠幩孮偺孮娫偵嵎偼擣傔傜傟側偄丅
丂帺慠巰摦暔乮昞侾俆乯丗梇偱偼丄壓悅懱偺怓慺寵惈態庮丄暃恡偺僋儘乕儉恊榓惈嵶朎庮媦傃惛憙偺娫幙嵶朎庮側偳偺弌尰偑懡偔尒傜傟傞偑丄孮娫偵堦掕偺孹岦傪尒側偄丅帗偱偼丄壓悅懱偺怓慺寵惈態庮丄暃恡偺僋儘乕儉恊榓惈嵶朎庮側偳偺敪尰傪尒傞丅側偍丄俼亅俀孮偺侾椺偵旂壓怐偺慇堐態娻偑攛丄娞憻丄恡憻傊偺揮堏憸傪擣傔傞丅帗偺庮釃偺敪尰悢偁傞偄偼偦偺撪梕偵偮偄偰尒傞偲梇偲摨條偵孮娫偵嵎傪擣傔側偄丅
丂帺慠巰摦暔媦傃掕婜夝朥摦暔乮昞侾俇乯丗俇丄侾俀丄侾俉媦傃俀係儢寧栚偵掕婜揑偵夝朥偟偨摦暔偲帺慠巰摦暔偺庮釃敪尰偵偮偄偰偼丄専嵏懳徾摦暔偲偟偰梇偱偼俶亅俀孮丄俼亅俀孮丄俶亅俆孮媦傃俼亅俆孮偱偦傟偧傟俀俈丄俀俋丄俀俉媦傃俀俇椺丄帗偱偼偦傟偧傟俀俈丄俀俈丄俁侽媦傃俀俋椺偱偁傞丅側偍丄梇偺俶亅俀孮丄俼亅俀孮丄俶亅俆孮媦傃俼亅俆孮偱偦傟偧傟俁丄侾丄俀媦傃係椺丄帗偺俶亅俀孮媦傃俼亅俀孮偺奺乆俁椺偲俼亅俆孮偺侾椺偼丄巰屻曄壔偑嫮偔専嵏晄擻偱偁偭偨丅
丂梇偱嵟傕庮釃敪尰偑懡偔擣傔傜傟傞憻婍偼惛憙偱偁傝俶亅俀孮丄俼亅俀孮丄俶亅俆孮媦傃俼亅俆孮偱偦傟偧傟俋丄俈丄俉媦傃俉椺偱偁傞丅
丂師偄偱暃恡偺僋儘乕儉恊榓惈嵶朎庮偑奺孮偦傟偧傟俀丄俁丄係媦傃俀椺偵尒傜傟傞丅偦偺奜丄壓悅懱偱怓慺寵惈態庮偑俶亅俀孮偱俀椺丄俼亅俀孮媦傃俶亅俆孮偱奺乆侾椺偢偮丄傑偨峛忬態偺態庮偑俶亅俆孮偱侾椺偵擣傔傜傟傞丅
丂帗偱偼丄暃恡偱僋儘乕儉恊榓惈嵶朎庮偑俶亅俀孮丄俼亅俀孮媦傃俶亅俆孮偱偦傟偧傟俁丄侾媦傃俀椺偵丄師偄偱壓悅懱偺怓慺寵惈態庮偑俶亅俀孮丄俼亅俀孮媦傃俼亅俆孮偱奺乆侾椺偢偮丄俶亅俆孮偱俀椺偵擣傔傜傟傞丅偦偺奜偺憻婍偱偼峛忬態偺曃暯忋旂娻偑俶亅俀孮媦傃俼亅俀孮偱奺乆侾椺丄銪憻偺儕儞僷庮偑俶亅俆孮偱侾椺丄堓偺慇堐擏庮偑俼亅俆孮偱侾椺偵擣傔傜傟傞丅傑偨丄旂壓怐媦傃擕態偱偼擷態庮偑俶亅俆孮偱侾椺丄態娻偑俶亅俀孮媦傃俶亅俆孮偱奺侾椺丄慇堐庮偑俶亅俆孮偱俀椺偵丄慇堐態娻媦傃儕儞僷慻怐偺儕儞僷庮偑俼亅俀孮偱偦傟偧傟侾椺偢偮擣傔傜傟傞丅偙傟傜偺庮釃敪尰摦暔悢偼丄梇偱偼俶亅俀孮丄俼亅俀孮丄俶亅俆孮媦傃俼亅俆孮偱偦傟偧傟侾侾丄俋丄俋媦傃俉椺偱偁傝丄帗偱偼偦傟偧傟係丄俆丄俉偍傛傃俀椺偱偁傞丅
丂忋弎偺傛偆偵庮釃偺慻怐妛揑専嵏偺寢壥丄梇帗偲傕偵庮釃偺敪尰悢丄敪尰晹埵偁傞偄偼慻怐妛揑専嵏偱堦掕偺孹岦偼擣傔傜傟偢丄偐偮孮娫偵柧傜偐側嵎偼擣傔傜傟側偄丅
丂兞慄徠幩僂僀儞僫乕僜乕僙乕僕偺埨慡惈傪挷傋傞栚揑偱儔僢僩偵傛傞俀係儢寧娫偺枬惈撆惈帋尡傪峴偭偨丅
丂堦斒徢忬丄愛塧検媦傃巰朣棪偱偼丄梇帗偲傕偵俀係儢寧娫偵榡偭偰摨堦揧壛検偵傛傞旕徠幩孮偲徠幩孮偺娫偵柧傜偐側嵎偼擣傔傜傟側偄偑丄帗偺惉挿嬋慄偱俈侽廡栚埲崀俶亅俆孮偑俼亅俆孮偵斾傋傗傗憹壛偺孹岦傪帵偡丅傑偨丄掕婜揑偵峴偭偨寣塼宍懺妛揑専嵏媦傃寣惔惗壔妛揑専嵏偺奺帪婜偱庒姳偺桳堄嵎傪帵偡崁栚傪擣傔傞偑丄梇帗偲傕偵摨堦揧壛検偺旕徠幩孮偲徠幩孮偺娫偵柧傜偐側孹岦偼擣傔傜傟側偄丅傑偨丄昦棟妛揑専嵏偱偼丄偦偺憻婍廳検媦傃庮釃敪尰悢偵傕梇帗偲傕偵柧傜偐側嵎偼擣傔傜傟側偄丅側偍丄搑拞帺慠巰摦暔偺専嵏偱傕庮釃敪尰悢偵嵎偼擣傔傜傟側偄丅
丂埲忋丄兞慄徠幩僂僀儞僫乕僜乕僙乕僕傪儔僢僩偵搳梌偟偰傕丄崱夞偺忦審壓偱偼徠幩偵傛傞偲尒側偝傟傞塭嬁偼擣傔傜傟側偄丅
丂兞慄徠幩僂僀儞僫乕僜乕僙乕僕偺埨慡惈傪挷傋傞栚揑偱丄僒儖偵傛傞俀係儢寧娫偺枬惈撆惈帋尡傪峴偭偨偺偱丄偦偺寢壥偵偮偄偰曬崘偡傞丅
丂幚尡偵梡偄偨僂僀儞僫乕僜乕僙乕僕偼丄崅嶈僴儉惢偱丄擔杮尨巕椡尋媶強崅嶈尋媶強偵偍偄偰俇侽侽倠倰倎倓偺兞慄徠幩傪峴偭偨丅偦偺屻搥寢姡憞偟丄偙傟傪専懱偲偟偰俆倵乛倵亾偺妱偵慏嫶擾応惢僒儖帞堢梡屌宆帞椏偵揧壛偟偨丅
丂惷壀導幚尡摦暔擾嬈嫤摨慻崌傛傝丄専塽偢傒偺僀儞僪嶻傾僇僎僓儖傪峸擖偟丄僒儖帞堢幒乮壏搙丗俀俁亇侾亷丄幖搙丗俆俆亇俆亾丄徠柧丗侾俀帪娫柧丄侾俀帪娫埫乯偵偰幚尡奐巒傑偱撻壔帞堢偟偨丅
丂寬峃偲巚傢傟傞傾僇僎僓儖梇帗奺俇摢乮寁侾俀摢乯傪侾孮俁摢偐傜側傞俀孮偵暘偗丄侾孮偵偼徠幩傪峴傢側偐偭偨僂僀儞僫乕僜乕僙乕僕乮俶孮乯丄懠偺侾孮偵偼徠幩僂僀儞僫乕僜乕僙乕僕乮俼孮乯傪揧壛偟偨帞椏傪梌偊偨丅媼塧偼枅擔屵慜侾侾帪偵屌宆帞椏傪侾摢摉偨傝侾俆侽倗梌偊偨丅偝傜偵廡俀夞價僞儈儞俠傪侾夞俆侽倣倗僠儑僐儗乕僩偵揧壛偟偰梌偊偨丅堸悈偼帺摦媼悈憰抲偵傛傝帺桼偵愛庢偝偣偨丅
丂堦斒徢忬偼枅擔媼塧慜偵娤嶡偟丄懱廳應掕偼寧侾夞峴偭偨丅
丂幚尡奐巒慜偍傛傃幚尡奐巒屻俁丄俇丄俋丄侾俀丄侾俆丄侾俉丄俀侾偍傛傃俀係儢寧娫栚偵丄暁嵼惷柆傛傝嵦寣偟丄寣塼宍懺妛揑専嵏偍傛傃寣惔惗壔妛揑専嵏傪峴偭偨丅
丂寣塼宍懺妛揑専嵏偲偟偰偼丄敀寣媴悢乮倂俛俠乯丆愒寣媴悢乮俼俛俠乯丆僿儌僌儘價儞検乮俫倐乯丆僿儅僩僋儕僢僩抣乮俫倲乯丄暯嬒愒寣媴梕愊乮俵俠俛乯丆暯嬒愒寣媴怓慺検乮俵俠俫乯丆暯嬒愒寣媴寣怓慺擹搙乮俵俠俫俠乯丆寣彫斅悢乮俹俴俿乯丆寣彫斅梕愊斾乮俹們倲乯偍傛傃暯嬒寣彫斅梕愊乮俵俹倁乯偵偮偄偰俠倧倳倢倲倕倰丂俠倧倳値倲倕倰丂倣倧倓倕倢丂俽俹傪梡偄偰應掕偟偨丅偝傜偵揾枙昗杮乮僊儉僓愼怓乯傪嶌惉偟偰敀寣媴昐暘斾傪悢偊偨丅寣惔惗壔妛揑専嵏偱偼丄嵦寣屻暘棧偟偨寣惔偵偮偄偰俧倕倣倱倎倕們係宆僆乕僩傾僫儔僀僓乕傪梡偄偰丄憤僞儞僷僋検乮俿亅俹俼俷丆榓岝僉僢僩丂乯丄傾儖僽儈儞検乮俙俴俛丄榓岝僉僢僩乯丄擜慺拏慺乮俛倀俶丆僔僲僥僗僩乯丄僋儗傾僠僯儞乮俠俼俶丆俛俵倄僉僢僩乯丄寣摐抣乮俧俴倀丆俛俵倄僉僢僩乯丄儕儞帀幙乮俹俬丆榓岝僉僢僩乯丄僩儕僌儕僙儔僀僪乮俿亅俧俴倄丆俛俵倄僉僢僩乯丄憤僐儗僗僥儘乕儖乮俿亅俠俫俷丆俛俵倄僉僢僩乯丄傾儖僇儕惈儂僗僼傽僞乕僛乮俙俴俹丄榓岝僉僢僩乯丄僐儕儞僄僗僥儔乕僛乮俠俫亅俤丆俛俵倄僉僢僩乯丄僋儗傾僠儞僉僫乕僛乮俠俲丆俛俵倄僉僢僩乯丄僩儔儞僗傾儈僫乕僛乮俧俷俿丆俧俹俿丆塰尋僉僢僩乯丄兞亅僌儖僞儈乕儖僩儔儞僗儁僾僠僞乕僛乮兞亅俧俿俹丆俛俵倄僉僢僩乯丄兛亅僴僀僪儘僉僔僽僠儗僀僩僨僴僀僪儘僎僫乕僛乮俫俛俢俫丆俛俵倄僉僢僩乯丄擕巁扙悈慺峺慺乮俴俢俫亅俹丆僔僲僥僗僩乯丄偝傜偵揹夝幙偲偟偰僇儖僔僂儉乮俠倎丄榓岝僉僢僩乯丄柍婡儕儞乮俹倝丄榓岝僉僢僩乯偍傛傃儅僌僱僔僂儉乮俵倗丆榓岝僉僢僩乯傪丄傑偨擔棫揹夝幙帺摦暘愅婡俈侽俀宆偱僫僩儕僂儉乮俶倎乯丆僇儕僂儉乮俲乯偍傛傃僋儘乕儖乮俠倢乯傪應掕偟偨丅
丂幚尡廔椆帪偺俀係儢寧栚偵墫巁働僞儈儞杻悓壓偱栩摦柆傛傝曻寣抳巰偝偣丄昦棟夝朥傪峴偭偨丅奺揈弌憻婍偺擏娽揑娤嶡傪峴偄丄憻婍廳検傪應掕偟偨乮擼丄怱憻丄攛丄娞憻丄恡憻丄銪憻丄惛憙丄棏憙丄壓悅懱丄峛忬態丄暃恡乯丅憻婍偼侾侽亾拞惈儂儖儅儕儞塼偵屌掕偟偨屻丄忢朄偵廬偭偰俫亅俤愼怓傪巤偟丄慻怐妛揑専嵏偵嫙偟偨丅専嵏偟偨憻婍偼丄忋婰偺懠偵丄妠壓態丄嫻態丄愩丄怘摴丄堓丄彫挵丄戝挵丄鋁憻丄惛憙忋懱丄惛擷丄慜棫態丂丄巕媨丄銷泖丄崪悜乮戝戁崪乯丄愐悜丄枛徑恄宱乮嵗崪恄宱乯丄儕儞僷愡丄旂晢偍傛傃嬝擏乮戝戁晹乯偱偁傞丅
丂俋儢寧栚偵巰朣偟偨帗偺俶孮偺侾摢乮俶亅俁乯偍傛傃侾俉儢寧栚偵巰朣偟偨梇偺俶孮偺侾摢乮俶亅俀乯傪彍偄偰丄懠偺侾侽摢偵偼帪乆壓棢徢忬傪擣傔偨偑丄孮娫偵嵎偼傒傜傟側偐偭偨丅
丂侾俉儢寧栚偵巰朣偟偨梇偺侾摢乮俶亅俀乯偼丄侾俈儢寧栚崰傛傝怘梸尭戅丄擜摐乮僽僪僂摐帋尡巻梲惈乯側偳偺徢忬偲嫟偵嵍慜屻巿偵杻醿徢忬傪掓偟丄師戞偵憠嶍偲寉搙偺昻寣徢忬傪擣傔傞偵帄偭偨丅敪徢屻俁廡娫崰傛傝慡恎惈偺醶澒傪偍偙偟偨丅醶澒偼娫寚揑偱屇媧崲擄傪敽偭偰偍傝屻媩斀挘傪掓偟偨丅偦偟偰敪徢屻侾丏俆儢寧偱巰朣偟偨丅
丂俋儢寧栚偵巰朣偟偨帗偺侾摢乮俶亅俁乯偼俉儢寧栚崰傛傝怘梸尭戅丄壓棢側偳偺徢忬偑懕偒丄俋儢寧栚偵憠嶍丄昻寣丄怘梸攑愨側偳偺徢忬偑傒傜傟巰朣偟偨丅
丂僀乯梇乮恾侾乯丗俶亅侾偼搳梌奐巒屻偐傜丄侾侽儢寧栚傑偱偲俀侽儢寧栚偵備傞傗偐側憹壛偑傒傜傟偨丅俶亅俀偼丄慜弎偺徢忬偑敪尰偡傞傑偱挊柧側憹尭傪帵偝側偐偭偨丅偟偐偟敪徢屻挊柧側尭彮偑傒傜傟丄巰朣帪偺懱廳偼係丏係俆倠倗偱偁偭偨丅俶亅俁偼幚尡婜娫拞憹壛傪懕偗偨丅
丂俼孮偱偼俼亅俇偑俀俀儢寧栚傛傝尭彮偡傞孹岦傪帵偟偨偑丄懠偺俀摢偼幚尡婜娫拞憹壛傪擣傔偨丅
丂儘乯帗乮恾俀乯丗俶亅侾偲俶亅俀偼幚尡婜娫拞挊柧側憹尭傪帵偝側偐偭偨丅巰朣偟偨俶亅俁偼丄俇儢寧栚埲屻尭彮傪帵偟丄巰朣帪偺懱廳偼俁丏係俆倠倗偱偁偭偨丅
丂俼孮偱偼俼亅俇偼幚尡婜娫拞懱廳偺墶攪偄傪帵偟憹尭偼傒傜傟側偐偭偨偑丄俼亅係偍傛傃俼亅俆偼侾俁儢寧栚崰傛傝憹壛傪帵偟偨丅
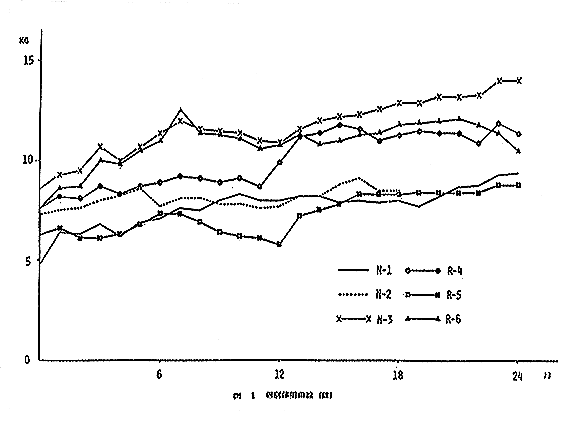 |
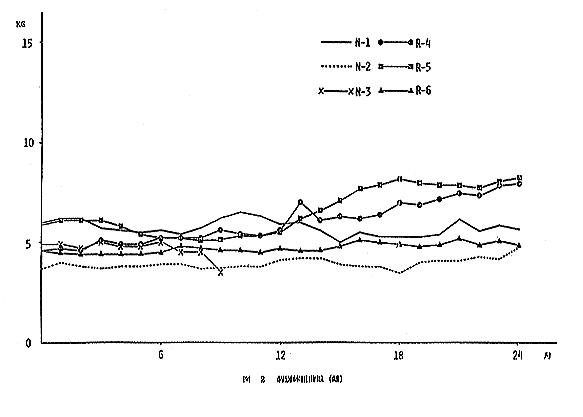 |
丂梇偺俼孮偺敀寣媴悢偑俇儢寧栚偱俶孮偵斾傋憹壛偡傞孹岦傪帵偡偑桳堄嵎偼擣傔傜傟側偄丅傑偨俼俛俠丆俫倐丆俫倲偑俇儢寧栚偺帗偺俼孮偱桳堄側憹壛傪帵偡丅
丂俋儢寧栚偱丄梇偺俼孮偱倂俛俠偺憹壛偑擣傔傜傟傞丅
丂傑偨侾俉偍傛傃俀侾儢寧栚偱梇偺俼孮偺俹俴俿偍傛傃帗偺俼孮偺俵俠俫俠偵桳堄偺憹壛偑擣傔傜傟傞丅
丂敀寣媴昐暘斾偱偼丄侾俆儢寧栚偱梇偺俼孮偑扨媴偑桳堄偵憹壛偡傞埲奜丄梇帗嫟偵俶孮偲斾傋俼孮偵桳堄偺嵎偼傒傜傟側偄丅
丂俁儢寧栚偱丄梇偺俶孮偵俿亅俹俼俷丆俙俴俛丆俠俲丆兞亅俧俿俹丆俠倎丆俹倝偍傛傃俶倎偵桳堄偺憹壛偁傞偄偼尭彮偑擣傔傜傟傞偑丄帗偱偼桳堄嵎偼擣傔傜傟側偄丅
丂俋儢寧栚偱偼丄帗偺俼孮偱俲偺憹壛偑擣傔傜傟傞偑丄搳梌慜偺抣偲斾傋傞偲堎忢抣偲偼峫偊傜傟側偄丅
丂侾俀儢寧栚偱偼丄梇偺俶孮偺俿亅俹俼俷偍傛傃俶倎丄傑偨帗偺俼孮偺俠俲偍傛傃俹倝偑桳堄偺尭彮傪帵偡丅
丂侾俆儢寧栚偱偼帗偺俼孮偵俧俷俿偍傛傃俠倢偺掅壓傑偨偼憹壛偑擣傔傜傟傞丅
丂侾俉儢寧栚埲崀偱偼丄俀侾儢寧栚偵帗偺俼孮偺俿亅俧俴倄偵憹壛偑擣傔傜傟傞丅
丂埲忋丄寣惔惗壔妛揑専嵏偱偼丄奺帪婜偱桳堄嵎傪擣傔傞崁栚偑偁傞偑丄慡婜娫傪捠偟偰堦掕偺孹岦傪掓偡傞傕偺偼擣傔傜傟側偄丅
丂乮倝乯憻婍廳検乮昞侾俁乯丗憻婍廳検偱偼丄幚廳検偍傛傃斾廳検偱丄帗梇嫟偵俶孮偍傛傃俼孮偺娫偱桳堄嵎傪帵偡憻婍偼擣傔傜傟側偐偭偨丅
丂乮倝倝乯擏娽強尒丗梇偺俶孮偱侾椺乮俶亅侾乯偵攛偺扽暡捑拝傪丄懠偺侾椺乮俶亅俁乯偱偼攛昞柺偵敀怓偺棽婲偑尒傜傟丄妱柺偱婥娗巟暻偺旍岤傪擣傔傞丅
丂帗偱偼丄俶孮偱俀椺乮俶亅侾丆俶亅俀乯偵攛偺扽暡捑拝傪擣傔丄偦偺撪侾椺乮俶亅侾乯偱偼攛偺擽釃偺宍惉偲嫻枌偲偺桙拝傪尒傞偲嫟偵丄嫻峯撪偵栺侾侽倣倢偺擕敀怓挷嫻悈偺挋棷傪擣傔傞丅
丂忋婰偺懠偵偼丄擏娽揑偵傎偲傫偳曄壔偼擣傔傜傟側偄丅
丂乮倝倝倝乯慻怐妛揑強尒乮昞侾係乯丗昞偵帵偡傛偆側曄壔偑傒傜傟傞偑丄偦偺敪惗悢偵偼孮娫偵偼嵎偼擣傔傜傟側偄丅
丂乮倝乯擏娽強尒
丂梇偺俶孮乮俶亅俀乯丗奜尒忋丄憠嶍丄壜帇擲枌偺憮敀壔偑尒傜傟丄嵍塃泓壓偍傛傃憀宎晹偵旂壓偺晜庮傪擣傔傞丅憻婍偱偼嵍塃戝擼慜摢梩悜幙晹偵弌寣憙偑尒傜傟丄偝傜偵戞俁擼幒偺奼挘傪擣傔傞丅傑偨攛偺扽暡捑拝偍傛傃怱擷塼偺挊柧側挋棷傪擣傔傞偑丄懠偺憻婍偵偼傎偲傫偳曄壔傪尒側偄丅
丂帗偺俶孮乮俶亅俁乯丗奜尒忋憠嶍偲娽豳偺晜庮傪擣傔丄暊晹旂壓慻怐偼堦晹僛儔僠儞條傪掓偡傞丅怱憻偼旍戝偟丄姤忬摦惷柆廃埻偵揰忬偁傞偄偼斄忬偺弌寣憙傪擣傔傞丅偦偺懠偵攛偺扽暡捑拝丄挵娫枌儕儞僷愡偺庮戝傪尒傞丅
丂乮倝倝乯慻怐妛揑強尒
丂帗偺俶孮乮俶亅俀乯丗戝擼悜幙偱挊柧側弌寣憙偑傒傜傟丄偦偺廃埻偺恄宱銹嵶朎偼丄庮戝丄憹怋偟丄婷怘憸乮僿儌僕僨儕儞乯傕擣傔傜傟傞丅弌寣憙廃埻偺擼幚幙偼嬻朎壔傪掓偡丅偟偐偟彫擼偵偼曄壔傪擣傔側偄丅
丂懠偵攛偺扽暡捑拝丄娞嵶朎偺朿壔偍傛傃恡偺偆偭寣傪尒傞丅
丂帗偺俶孮乮俶亅俁乯丗戝擼旂幙偵寣娗偺愷嵡丄恄宱銹嵶朎偺憹怋丄婾恄宱怘尰徾偍傛傃寉搙偺弌寣偑傒傜傟傞丅怱憻偱偼姤忬摦柆偺峓嵡偍傛傃怱嬝撪弌寣丄墌宍嵶朎偺怹弫丄怱嬝偺朿壔傪擣傔傞丅攛偱偼婥娗巟撪偵歕醾條暔偑傒傜傟丄攛朎撪偵偼丄朅枛嵶朎偺怹弫偍傛傃扽暡捑拝傪尒傞丅娞偱偼娞嵶朎偺嬻朎壔偍傛傃戝彫晄摨丄懡妀嵶朎偺憹壛丄椶摯偺奼挘傪傒傞丅偦偺傎偐丄暃恡旂幙偺弌寣丄悜幙偺愇奃捑拝傪尒傞丅
丂兞亅徠幩僂僀儞僫乕僜乕僙乕僕偺埨慡惈傪挷傋傞栚揑偱丄傾僇僎僓儖傪梡偄偨俀係儢寧娫偺枬惈撆惈帋尡傪峴偭偨丅
丂倎乯堦斒徢忬偍傛傃懱廳偱偼丄幚尡婜娫拞丄梇偍傛傃帗偺俶孮偵巰朣偑奺侾椺傒傜傟偨偑丄偦傟埲奜偼帗梇偲傕偵曄壔偼擣傔傜傟側偐偭偨丅
丂倐乯搳梌奐巒慜偍傛傃奐巒屻偺寣塼宍懺妛揑専嵏偍傛傃寣惔惗壔妛揑専嵏偱偼丄梇丄帗偲傕偵俼孮偱俶孮偲斾傋桳堄偺憹壛偁傞偄偼尭彮傪帵偡傕偺偑嶶尒偝傟傞偑丄宱帪揑偵傒傞偲堦掕偺孹岦偼擣傔傜傟側偄偙偲偐傜丄偄偢傟傕堦夁惈偺傕偺偲峫偊傜傟傞丅
丂們乯幚尡廔椆帪偺俀係儢寧栚偺昦棟妛揑専嵏偱傕徠幩偵傛傞偲巚傢傟傞昦曄偼擣傔傜傟側偐偭偨丅
丂倓乯搑拞巰朣偺巰場偼丄梇偺俶孮偺侾椺乮俶亅俀乯偱偼擼撪弌寣丄傑偨帗偺俶孮偺侾椺乮俶亅俁乯偼怱憻姤忬摦柆偺峓嵡偲恌抐偝傟偨丅
丂埲忋偺寢壥偐傜兞慄徠幩僂僀儞僫乕僜乕僙乕僕傪傾僇僎僓儖偵搳梌偟偰傕崱夞偺幚尡忦審壓偱偼徠幩偵傛傞偲巚傢傟傞塭嬁偼側偄傕偺偲峫偊傜傟傞丅
丂兞慄徠幩僂僀儞僫乕僜乕僙乕僕偺埨慡惈偵娭偡傞尋媶偺堦娐偲偟偰丄儅僂僗偵傛傞悽戙帋尡傪峴側偄丄奺悽戙偵偍偗傞斏怋惗棟抣偍傛傃嵜婏宍惈傊偺塭嬁傪専嶕偟偨丅
丂専懱偼丄旕徠幩乮侽倠倰倎倓乯偍傛傃徠幩乮俇侽侽倠倰倎倓乯僂僀儞僫乕僜乕僙乕僕傪巊梡偟偨丅僂僀儞僫乕僜乕僙乕僕乮埲壓僜乕僙乕僕偲棯乯偼壢妛媄弍挕怘昳徠幩尋媶塣塩夛媍巜掕偺傕偺傪梡偄偨丅
丂帞椏挷惢偼丄専懱偺僜乕僙乕僕傪敄偔僗儔僀僗偟偰搥寢姡憞偟偨屻乮曕巭傝俁俈丏俆亾乯丄暡嵱偟丄儅僂僗帞堢梡暡枛帞椏乮僆儕僄儞僞儖峺曣俲丏俲乯偵俆倵乛倵亾揧壛偟丄屌宆帞椏傪嶌惢偟偨丅傑偨丄懳徠偲偟偰偼儅僂僗帞堢梡屌宆帞椏乮僆儕僄儞僞儖峺曣俲丏俲乯傪梡偄偨丅
丂倓倓倄宯儅僂僗乮惷壀幚尡摦暔擾嬈嫤摨慻崌乯傪梡偄偨丅儅僂僗偼係廡椷偱峸擖偟丄侾廡娫撻壔帞堢乮壏搙俀俆亇侾亷丄幖搙俆侽亇俆亾丄侾俀帪娫恖岺徠柧乯屻丄幚尡偵嫙偟偨丅
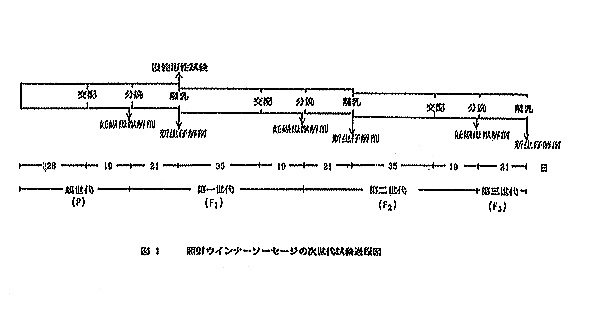
丂撻壔帞堢屻丄寬峃偲尒傜傟傞摦暔傪慖掕偟丄恊悽戙乮埲壓俹悽戙偲棯乯摦暔偲偟偰梇帗奺乆俆侽旵偐傜側傞懳徠孮丄旕徠幩孮偍傛傃徠幩孮偺俁孮偲偟偨丅俁孮偵暘偗偨摦暔偼丄恾侾偵帵偡慡婜娫丄懳徠孮偵偼帞堢梡帞椏傪丄旕徠幩孮偵偼旕徠幩僜乕僙乕僕揧壛帞椏傪丄徠幩孮偵偼徠幩僜乕僙乕僕揧壛帞椏傪帺桼偵愛庢偝偣偨丅
丂俹悽戙偺摦暔偼恾侾偵帵偡傛偆偵丄偦傟偧傟偺帞椏傪俀俉擔娫愛庢偝偣偨屻丄梇丗帗亖侾丗侾偱俁擔娫丄屵屻俆帪傛傝梻擔偺屵慜俋帪傑偱摨嫃偝偣岎攝傪峴側偭偨丅側偍丄摨嫃梻挬丄銼愷傪妋擣偟偨帗摦暔偼擠怭摦暔偲傒側偟丄偙偺擔傪擠怭侽擔偲偟偨丅擠怭摦暔偼俀暘偟丄侾孮偼擠怭侾俉擔栚偵枛婜戀巈専嵏偺偨傔偵朥専偟偨丅懠偺侾孮偼戞侾悽戙乮埲壓俥侾悽戙偲棯乯摦暔傪帺慠暘曍偝偣偨丅俥侾悽戙摦暔偼棧擕帪乮惗屻俀侾擔椷乯偱俁暘偟丄侾孮偼惗屻俀侾擔椷偱怴惗巈偺専嵏傪丄侾孮偼戞俀悽戙乮埲壓俥俀悽戙偲棯乯摦暔傪摼傞偨傔偵俆廡娫帞堢乆惉屻丄岎攝偝偣偨丅巆傝偺侾孮偼枬惈撆惈帋尡偺摦暔偵嫙偟偨丅偦偺屻偼恾侾偵帵偡偛偲偔戞俁悽戙乮埲壓俥俁悽戙偲棯乯傑偱幚尡傪峴側偭偨丅
丂側偍丄俥侾偍傛傃俥俀悽戙偱偺岎攝婜娫偼係擔娫偲偟偨丅
 |
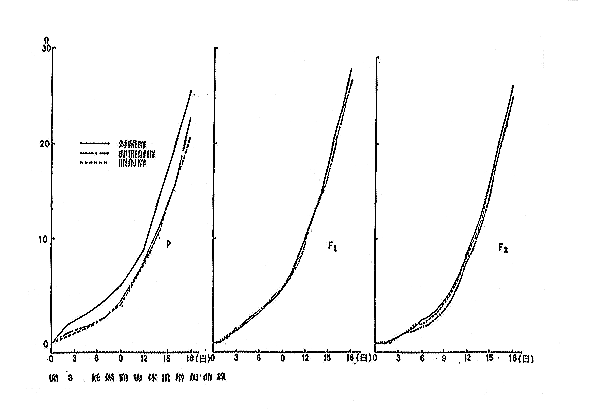
丂堦斒徢忬偼奜尒忋偺曄壔傪枅擔娤嶡偟偨丅懱廳應掕偼丄歁擕婜乮侽乣俁廡椷乯偺怴惗巈偱偼侾暊偛偲偵傑偲傔偰丄係廡椷傛傝岎攝帪傑偱偺婜娫偼屄乆偵丄偦傟偧傟廡侾夞應掕偟偨丅擠怭摦暔偼擠怭侽擔傛傝侾俉擔栚傑偱枅擔應掕偟丄擠怭侽擔傪婎偲偟偰懱廳偺憹壛検傪媮傔偨丅
丂斏怋惗棟抣偺巜昗偲偟偰
丂岎攝棪亖乮岎攝傪擣傔偨帗悢乛岎攝偵巊梡偟偨帗悢乯亊侾侽侽
丂擠怭棪亖乮擠怭摦暔悢乛岎攝傪擣傔偨摦暔悢乯亊侾侽侽
丂暯嬒摨暊巈悢亖帺慠暘曍偟偨摦暔偺摨暊巈悢
丂歁堢棪亖乮棧擕曣廱悢乛暘曍曣廱悢乯亊侾侽侽
丂棧擕棪亖乮憤棧擕巈悢乛憤弌嶻巈悢乯亊侾侽侽
丂偵偮偄偰専嶕偟偨丅
丂擠怭侾俉擔栚偺曣廱傪掗墹愗奐偟丄戀巈偺惗懚偺桳柍傪専嶕偟偨丅峏偵丄惗懚戀巈偼屄暿偵懱廳應掕丄岥峯撪傪娷傓奜宍専嵏偍傛傃敪堢抶墑戀巈乮懱廳侾倗埲壓乯傪専嵏偟偨丅巰朣戀巈偼忬懺偵傛傝怹擃戀巈丄戀斦堚巆偍傛傃拝彴嵀愓偺俁庬偵暘椶偟偨丅側偍丄拝彴悢偼惗懚戀巈悢偲巰朣戀巈悢偺崌寁偱昞傢偟偨丅
丂怴惗巈乮惗屻俀侾擔椷乯偺摦暔偵偮偄偰丄娞憻丄恡憻偍傛傃惛憙乮棏憙乯偺擏娽揑曄壔傪娤嶡偟偨屻丄廳検偺應掕傪峴側偭偨丅傑偨偦傟偧傟偵偮偄偰侾侽侽倗懱廳斾傪嶼弌偟偨丅
丂枛婜戀巈偍傛傃怴惗巈偼搄嶦夝朥屻傾儖僐乕儖屌掕偟丄俢倎倵倱倧値朄偵廬偄傾儕僓儕儞儗僢僪俽愼怓傪巤偟偰崪奿偺摟柧昗杮傪嶌惢偟丄崪奿偺堎忢側傜傃偵壔崪偺恑峴忬懺傪専嵏偟偨丅
丂俹悽戙摦暔偺撪丄俥侾悽戙偺恊摦暔偲偟偰梡偄偨巈傪暘曍偟偨摦暔乮梇帗乯偵偮偄偰丄屻偵弎傋傞棟桼偵傛傝崪奿愼怓傪峴側偄崢捙偺愬捙壔偵偮偄偰専嵏偟偨丅
丂奺應掕抣偺悇寁張棟偼丄侽乣俋廡椷乮岎攝帪乯傑偱偺摦暔偍傛傃擠怭摦暔偺懱廳丄暯嬒拝彴悢丄摨暊巈悢偍傛傃壔崪恑峴搙乮愬捙亄旜捙悢乯偼倲専掕丄戀巈懱廳偍傛傃憻婍廳検偼倂倕倝倢偺倂倕倝倗倛倲倝値倗丂俥倎們倲倧倰傪梡偄偨倲専掕丄岎攝棪丄擠怭棪丄歁堢棪丄棧擕棪偍傛傃俹悽戙恊摦暔偺崪奿専嵏惉愌乮崢捙偺愬捙壔乯偼冊丒俤乮俀乯専掕丄奜宍堎忢戀巈悢丄巰朣戀巈悢偍傛傃戀巈側傜傃偵怴惗巈偺崪奿専嵏惉愌偼倂倝倢們倧倶倧値偺弴埵榓専掕傪峴側偭偨丅
丂側偍丄偙傟傜偺専掕偼懳徠孮偲旕徠幩孮偍傛傃徠幩孮丄旕徠幩孮偲徠幩孮偺孮娫偱峴側偭偨丅
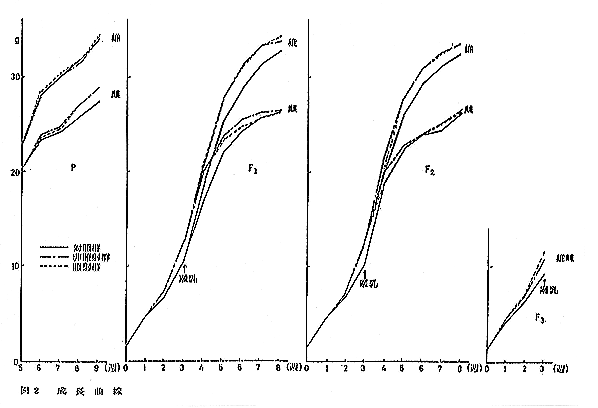
丂奺悽戙偲傕丄旕徠幩偍傛傃徠幩孮偱偼摦暔偑戝偒偔丄懳徠孮偵斾傋旍枮孹岦偑娤嶡偝傟傞丅
丂俹悽戙丗梇偱偼孮娫偵嵎偼擣傔側偄丅梇偼俇廡椷埲屻偵旕徠幩偍傛傃徠幩孮偱懳徠孮傪忋夞傞憹壛孹岦傪帵偡丅
丂俥侾悽戙丗侽乣俁廡椷乮摨暊扨埵偱應掕乯偱偼丄旕徠幩偍傛傃徠幩孮偱懳徠孮偵斾傋俀廡傛傝憹壛孹岦傪帵偟丄俁廡偱偼桳堄嵎傪擣傔傞丅旕徠幩孮偲徠幩孮偺娫偵偼嵎偼擣傔側偄丅
丂係乣俉廡椷偱偼丄梇偼懳徠孮偵斾傋旕徠幩偍傛傃徠幩孮偱憹壛孹岦傪帵偟丄旕徠幩孮偱偼係乣俈廡椷偱丄徠幩孮偱偼係乣俉廡椷偱桳堄嵎傪擣傔傞丅傑偨丄帗偱傕摨條偺孹岦傪擣傔傞丅偟偐偟丄梇帗偲傕旕徠幩孮偲徠幩孮偺娫偵偼柧傜偐側嵎偼擣傔側偄丅
丂俥俀悽戙丗俥侾悽戙偲摨條偺惉挿嬋慄傪帵偡丅侽乣俁廡椷偱偼丄俀廡椷傛傝懳徠孮偵斾傋旕懳徠偍傛傃徠幩孮偱憹壛孹岦傪帵偟丄俁廡偱偼桳堄嵎傪擣傔傞丅係乣俉廡椷偱偼丄梇偺旕徠幩孮偱係乣俈廡丄徠幩孮偺俇廡偱桳堄偵崅抣傪帵偡丅帗偼孮娫偵桳堄嵎傪擣傔側偄丅旕徠幩孮偲徠幩孮偺娫偵偼慡婜娫傪捠偟丄梇帗偲傕杦傫偳嵎傪擣傔側偄丅
丂俥俁悽戙丗俥侾偍傛傃俥俀悽戙偲摨條丄懳徠孮偵斾傋旕徠幩偍傛傃徠幩孮偱偼憹壛孹岦傪帵偡丅桳堄嵎偼俁廡椷偺懳徠孮偲徠幩孮偺娫偵擣傔傜傟傞丅旕徠幩孮偲徠幩孮偺娫偵偼杦傫偳嵎傪擣傔側偄丅
 |
丂俹悽戙丗懳徠孮偵斾傋旕徠幩偍傛傃徠幩孮偲傕俀擔栚傛傝柧傜偐偵掅抣傪帵偡丅旕徠幩孮偲徠幩孮偺娫偵偼杦傫偳嵎傪擣傔側偄丅
丂俥侾偍傛傃俥俀悽戙丗俁孮娫偵杦傫偳嵎傪擣傔側偄丅
 |
丂俹偍傛傃俥侾悽戙丗専嵏崁栚偵傛傝孮娫偵懡彮偺嵎偼擣傔傞偑丄偄偢傟偺専嵏崁栚偱傕桳堄嵎偼擣傔傜傟側偄丅
丂俥俀悽戙丗歁堢棪偍傛傃棧擕棪偼懳徠孮偵斾傋旕徠幩偍傛傃徠幩孮偱崅抣傪帵偡孹岦傪擣傔丄摿偵歁堢棪偱偼桳堄嵎傪擣傔傞丅
丂俹悽戙丗偄偢傟偺専嵏崁栚偱傕孮娫偵柧傜偐側嵎偼擣傔傜傟側偄丅偟偐偟丄巰朣戀巈悢偼懳徠孮偵斾傋旕徠幩孮偱掅抣傪帵偡孹岦傪擣傔傞丅側偍丄徠幩孮偱侾椺擣傔傜傟傞奜宍堎忢戀巈偼擼僿儖僯傾偱偁傞丅
丂俥侾悽戙丗暯嬒拝彴悢偼懳徠孮偵斾傋旕徠幩偍傛傃徠幩孮偱崅抣傪帵偟丄旕徠幩孮偼桳堄嵎傪擣傔傞丅偙偺懠丄奜宍堎忢戀巈悢偑懳徠孮偵斾傋旕徠幩孮偱崅抣傪丄憤巰朣戀巈悢偑懳徠偍傛傃旕徠幩孮偵斾傋徠幩孮偱傗傗掅抣傪帵偡丅偟偐偟丄偄偢傟傕桳堄嵎偼擣傔側偄丅奜宍堎忢戀巈偼旕徠幩孮偺旂壓弌寣侾椺傪彍偄偰慡椺撪斀懌偱偁傞丅
丂俥俀悽戙丗偄偢傟偺崁栚偱傕丄孮娫偵杦傫偳嵎傪擣傔側偄丅側偍丄奜宍堎忢戀巈偼懳徠孮偱旂壓弌寣偍傛傃撪斀懌傪奺侾椺丄旕徠幩孮偱撪斀懌侾椺傪擣傔傞丅
丂僀乯擏娽揑曄壔丗俥侾悽戙偱偼丄徠幩孮偺侾椺偵惛憙偺嵍塃晄懳徧傪擣傔傞丅俥俀悽戙偱偼丄旕徠幩孮偺梇偺俀椺偵恡憻寚懝乮曅懁惈乯傪擣傔傞丅俥俁悽戙偱偼丄懳徠孮偺梇偺俀椺偵恡憻偺悈朅宍惉傪擣傔傞丅
丂儘乯憻婍廳検乮昞俁乯丗奺悽戙偺梇帗偲傕丄懳徠孮偵斾傋旕徠幩偍傛傃徠幩孮偱娞憻廳検偺桳堄偺憹壛偁傞偄偼偦偺孹岦傪擣傔傞丅傑偨丄俥俁悽戙偱偼惛憙廳検偵摨條偺孹岦偑擣傔傜傟傞丅
丂俥侾悽戙丗壔崪恑峴搙乮纟崪丒嫍崪偺崪壔偍傛傃驿崪拞愡偺崪壔乯偑懳徠孮偵斾傋旕徠幩偍傛傃徠幩孮偱鈉乆掅抣傪帵偡丅
丂俥俀悽戙丗寊榏偑懳徠偍傛傃旕徠幩孮偵斾傋徠幩孮偱掅抣傪帵偡孹岦傪擣傔傞丅傑偨丄壔崪恑峴搙偱偼纟崪丄嫍崪偺崪壔偑懳徠孮偵斾傋旕徠幩偍傛傃徠幩孮偱嬐偐偵掅抣傪丄嫍崪拞愡偺崪壔偑懳徠偍傛傃旕徠幩孮偵斾傋徠幩孮偱嬐偐偵崅抣傪帵偡丅偟偐偟丄偄偢傟偺崁栚偱傕孮娫偵桳堄嵎傪擣傔側偄丅
丂俥俁悽戙丗寊榏偑懳徠孮偵斾傋旕徠幩孮偱丄崢捙偺愬捙壔偑懳徠偍傛傃旕徠幩孮偵斾傋徠幩孮偱丄纟崪丒嫍崪偍傛傃驿崪拞愡偺崪壔偑懳徠孮偵斾傋旕徠幩偍傛傃徠幩孮偱丄偄偢傟傕崅抣傪帵偡孹岦傪擣傔傞丅偟偐偟丄偄偢傟偺崁栚偱傕孮娫偵桳堄嵎偼擣傔側偄丅
丂俥侾悽戙丗偄偢傟偺崁栚偱傕孮娫偵杦傫偳嵎傪擣傔側偄丅
丂俥俀悽戙丗愬捙亄旜捙悢偑懳徠孮偵斾傋旕徠幩偍傛傃徠幩孮偱桳堄偵掅抣傪帵偡丅崢捙偺愬捙壔偼懳徠孮偵斾傋徠幩孮偱崅抣傪帵偡孹岦傪擣傔傞丅偟偐偟丄偄偢傟偺崁栚傕旕徠幩孮偲徠幩孮偺娫偵偼杦傫偳嵎傪擣傔側偄丅
丂俥俁悽戙丗崢捙偺愬捙壔偑懳徠偍傛傃旕徠幩孮偵斾傋徠幩孮偱崅抣傪帵偡孹岦傪擣傔丄旕徠幩孮偲偺娫偵桳堄嵎偑擣傔傜傟傞丅偙偺懠偺崁栚偱偼孮娫偵柧傜偐側嵎偼擣傔側偄丅
丂俹悽戙摦暔偺偆偪丄俥侾悽戙偺恊摦暔偵巊梡偟偨巈乮岎攝偵梡偄偨摦暔乯傪暘曍偟偨摦暔偵偮偄偰丄崢捙偺愬捙壔傪専嵏偟偨寢壥丄懳徠偍傛傃旕徠幩孮偵斾傋徠幩孮偱偼岎攝偟偨梇帗偺偆偪堦曽偁傞偄偼椉幰偵崢捙偺愬捙壔傪擣傔傞慻崌偣悢偑懡偔娤嶡偝傟傞乮昞俇乯丅傑偨丄俥俁悽戙摦暔偺偆偪怴惗巈偺崪奿専嵏傪峴側偭偨摦暔傪暘曍偟偨俥俀悽戙摦暔傪慿傝丄俹悽戙摦暔偵偮偄偰崢捙偺愬捙壔傪専嵏偟偨丅徠幩孮偱偼懳徠偍傛傃旕徠幩孮偵斾傋崢捙偺愬捙壔傪擣傔傞岎攝慻悢偑崅昿搙偱擣傔傜傟傞乮昞俈乯丅堦曽丄俹悽戙偱愬捙壔偑擣傔傜傟側偄摦暔偩偗偺慻崌偣偵傛偭偰摼傜傟偨俥俁悽戙乮怴惗巈乯偱偼愬捙壔偼侾椺傕擣傔傜傟側偄丅
丂徠幩僂僀儞僫乕僜乕僙乕僕偺斏怋惗棟偵偍傛傏偡塭嬁側傜傃偵嵜婏宍惈偺桳柍傪挷傋傞栚揑偱儅僂僗偵傛傞楢懕俁戙偺悽戙帋尡傪峴側偭偨丅
丂奺悽戙偲傕丄惉挿嬋慄丄擠怭曣廱懱廳憹壛嬋慄丄斏怋惗棟抣丄擠怭枛婜戀巈傊偺塭嬁偍傛傃怴惗巈偺憻婍廳検偺専嵏偱偼旕徠幩孮偲徠幩孮偲偺娫偵嵎偼擣傔傜傟偢丄徠幩僂僀儞僫乕僜乕僙乕僕愛庢偵傛傞塭嬁偼擣傔傜傟側偐偭偨丅擠怭枛婜戀巈偍傛傃怴惗巈偺崪奿専嵏偱偼丄崢捙偺愬捙壔偑俥俁悽戙乮枛婜戀巈偍傛傃怴惗巈乯偱懳徠偍傛傃旕徠幩孮偵斾傋徠幩孮偱崅抣傪帵偡孹岦傪擣傔偨丅偙傟偼丄徠幩孮偱偼俹悽戙偵愬捙壔傪擣傔偨摦暔偺岎攝偑懠偺孮偵斾傋崅棪偵峴側傢傟偰偄傞偙偲丄堦曽丄俹悽戙偱愬捙壔傪擣傔側偄摦暔偺岎攝偺慻崌偣傪帩偮俥俁偺怴惗巈偱偼丄愬捙壔傪侾椺傕擣傔側偄偙偲傛傝丄俥俁悽戙偺徠幩孮偱愬捙壔偑崅棪偵擣傔傜傟傞偺偼俹悽戙偵愬捙壔傪擣傔偨摦暔偺岎攝偑懠偺孮偵斾傋偨傑偨傑崅棪偱偁偭偨偙偲偵婲場偡傞偲峫偊傜傟傞丅
丂埲忋偺偙偲傛傝丄杮幚尡忦審壓偱徠幩僂僀儞僫乕僜乕僙乕僕愛庢偵傛傞塭嬁偼擣傔傜傟側偐偭偨丅
丂側偍丄俥侾悽戙摦暔傪梡偄偨枬惈撆惈帋尡偱偼丄摦暔帞堢幒偺娐嫬場巕偑尨場偲峫偊傜傟傞搑拞巰朣摦暔偑奺孮偲傕崅棪偵敪惗偟偨偨傔乮俀係儢寧栚偺椵愊巰朣棪丗梇偺懳徠俉侽丏侽亾丄旕徠幩俇俉丏俁亾丄徠幩俉俀亾丄帗偺懳徠俉俇丏侽亾丄旕徠幩俉俋丏俈亾丄徠幩俉俉丏俉亾乯枬惈撆惈帋尡偺栚揑傪払偡傞偙偲偑偱偒側偐偭偨偺偱丄怴偨偵摦暔傪峸擖偟偰幚巤偟偨丅
丂徠幩怘昳偵偮偄偰堚揱妛揑埨慡惈傪昡壙偡傞偨傔偵偼帋尡朄偺慖戰偑偒傢傔偰廳梫偱偁傞丅悢懡偔偺堚揱撆惈帋尡偺偆偪偳傟傪庢傝忋偘傞傋偒偐偵偮偄偰偼丄帋尡懳徾偺廳梫搙偵墳偠偰攝椂偝傟傞傋偒偱偁傠偆偑丄僂僀儞僫乕僜乕僙乕僕偼偦偺徚旓検傕偐側傝戝偒偄偙偲傪峫椂偟偰丄岤惗徣偑岞偵偟偨乽怘昳揧壛暔側偳偺堚揱揑埨慡惈昡壙偺婎弨乿偵帵偝傟偨奺庬偺帋尡朄傪傎傏僇僶乕偡傞偵懌傝傞崁栚偺帋尡朄傪慖戰偟偨丅側偍歁擕摦暔傪梡偄傞摿掕嵗埵帋尡偼尰帪揰偵偍偄偰丄嵟傕怣棅偡傞偵懌傞帋尡朄偲偝傟偰偄傞偑丄偦偺幚巤偵偼敎戝側旓梡傪梫偟丄偟偐傕帋尡朄帺懱専摙偺梋抧偑戝偒偄偲偝傟偰偄傞揰傪峫椂偟偰崱夞偼幚巤傪尒憲偭偨丅徠幩怘昳偵偮偄偰歁擕摦暔偵傛傞摿掕嵗埵帋尡偑幚巤偝傟偨偲偄偆曬崘偼彅奜崙偵偍偄偰傕奆柍偱偁傝丄歁擕摦暔偵傛傞桪惈抳巰帋尡偺寢壥偑嵟傕廳帇偝傟偰偄傞偺偑尰忬偱偁傞丅
丂幚巤偟偨帋尡崁栚偼師偺捠傝偱偁傞丅
丂侾丏嵶嬠傪梡偄偨撍慠曄堎桿敪帋尡
丂丂丂侾乯嵶嬠偵懳偡傞撍慠曄堎桿敪帋尡
丂丂丂俀乯儅僂僗偵傛傞廻庡宱桼帋尡
丂俀丏歁擕摦暔攟梴嵶朎傪梡偄偨撍慠曄堎桿敪帋尡
丂丂丂侾乯愼怓懱堎忢帋尡乮帋尡娗撪乯
丂俁丏歁擕摦暔偺惗懱傪梡偄偨撍慠曄堎桿敪帋尡
丂丂丂侾乯愼怓懱堎忢帋尡乮儅僂僗惗懱偵傛傞彫妀帋尡乯
丂丂丂俀乯儅僂僗偵傛傞桪惈抳巰帋尡
丂専懱偺惢憿偼崅嶈僴儉姅偵埶棅偟丄徠幩偼擔杮尨巕椡尋媶強崅嶈尋媶強偱幚巤偟偨丅徠幩慄検偼侽丏俇俵倰倎倓乮侽丏俁俵倰倎倓乛帪乯丅専懱偼徠幩丒旕徠幩偲傕捈偪偵搥寢姡憞偟亅俀侽亷偱曐懚偟偨丅
丂乮僀乯専掕嬠丗俽倎倢倣倧値倕倢倢倎丂倲倷倫倛倝倣倳倰倝倳倣丂俿俙侾侽侽丆俿俙俋俉丆俿俙侾俆俁俆丆俿俙侾俆俁俈丆俿俙侾俆俁俉丆偍傛傃俤丏們倧倢倝丂倂俹俀丂倳倴倰俙傪巊梡偟偨丅
丂乮儘乯帋尡専懱丗徠幩偍傛傃旕徠幩僂僀儞僫乕僜乕僙乕僕偺搥寢姡憞暔傪悈傑偨偼恷巁僄僠儖偱拪弌偟偨傕偺傪帋尡帋椏偲偟偨丅
丂乮僴乯帋尡憖嶌朄丗僾儗乕僩朄乮俹倢倎倲倕丂倝値們倧倰倫倧倰倎倲倝倧
倣倕倲倛倧倓乯偵傛偭偨丅
丂帋尡寢壥偼昞俙亅侾偵帵偡偛偲偔偱丄俇嬠姅偺偡傋偰偵偮偄偰徠幩丒旕徠幩傪栤傢偢丄堿惈懳徠偵偔傜傋偰曄堎廤棊偺憹壛偼擣傔傜傟側偐偭偨丅
丂埲忋偺寢壥偐傜丄徠幩怘昳偼巊梡偟偨帋尡宯偵偮偄偰撍慠曄堎惈傪桳偟側偄傕偺偲寢榑偝傟傞丅
丂専掕嬠偲偟偰俽倎倢倣倧値倕倢倢倎丂倲倷倫倛倝倣倳倰倝倳倣丂俧係俇傪梡偄丄俛俢俥侾梇儅僂僗乮俀係乣俀俇倗乯偵徠幩偍傛傃旕徠幩僂僀儞僫乕僜乕僙乕僕偺拪弌暔乮悈偍傛傃僋儘儘儂儖儉丒儊僞僲乕儖拪弌暔傪崿崌乯侽丏俁倗傪侾夞暊峯撪搳梌偟偨丅
丂昞俙亅俀偵帵偡偛偲偔侾暯斅偁偨傝偺曄堎僐儘僯乕悢偵娭偟偰丄懳徠丄徠幩偍傛傃旕徠幩孮偺娫偵桳堄偺嵎偼擣傔傜傟側偐偭偨丅
丂僠儍僀僯乕僘丒僴儉僗僞乕偺戀巈嵶朎乮弶戙嵶朎乯偲僸僩偺儕儞僷媴偵丄僂僀儞僫乕僜乕僙乕僕偺悈拪弌暔傪嵟廔擹搙侾倣倗乛倣倢丆俀倣倗乛倣倢偵側傞傛偆偵攟抧偵壛偊丄俀係帪娫屻偵愼怓懱昗杮傪嶌惢偟偨丅娤嶡偼僴儉僗僞乕嵶朎偱偼侾侽侽屄丄僸僩儕儞僷媴偱偼俆侽屄偺暘楐拞婜憸偵偮偄偰峴側偭偨丅
丂徠幩丄旕徠幩偺偄偢傟偵偍偄偰傕丄桳堄側愼怓懱堎忢偺憹壛偼擣傔傜傟側偐偭偨丅
丂徠幩偍傛傃旕徠幩僂僀儞僫乕僜乕僙乕僕偺僋儘儘儂儖儉丗儊僞僲乕儖乮俀丗侾乯拪弌暔偲悈拪弌暔偺崿崌暔傪俛俢俥侾乮俋廡椷乯梇儅僂僗偵宱岥揑偵侾夞搳梌偟偨丅搳梌俀係帪娫屻偵搄嶦偟丄崪悜嵶朎偺揾枙昗杮傪嶌惢偟偨丅娤嶡偼儅僂僗侾旵偁偨傝侾俆侽侽屄偺懡愼惈愒寣媴傪僇僂儞僩偟丄偦偺拞偺彫妀傪桳偟偨懡愼惈愒寣媴偺弌尰昿搙傪媮傔偨丅
丂昞俙亅係偵帵偡偛偲偔徠幩偍傛傃旕徠幩孮偺偄偢傟偵偍偄偰傕彫妀偺桳堄側憹壛傪擣傔傜傟側偐偭偨丅
丂俛俢俥侾梇儅僂僗乮惷摦嫤乯偵懳偟偰傕俇廡椷偐傜侾係廡椷傑偱偺俉廡娫偵傢偨傝徠幩偍傛傃旕徠幩丄僂僀儞僫乕僜乕僙乕僕帞椏傪梌偊偨丅堿惈懳徠偵偼屌宆俷俵俥帞椏傪梌偊丄梲惈懳徠孮偼倣倕倲倛倷倢丂倣倕倲倛倎値倕倱倳倢倖倧値倎倲倕乮俵俵俽乯傪摨婜娫係擔枅偵侾夞乮寁侾係夞乯丄侾夞偵偮偒侾俀丏俆倣倗乛倠倗傪暊峯撪搳梌偟偨丅幚尡偵梡偄偨梇儅僂僗偼奺孮俁侽摢偲偟丄梲惈懳徠孮偺俀侽摢偲偟偨丅搳梌屻侾摢偺梇儅僂僗偵懳偟侾摢偺帗傪係擔娫偵傢偨傝岎攝偟丄偙偺岎攝傪俀夞偔傝曉偟偨丅岎攝屻擠怭拞婜偵帗儅僂僗傪搄嶦丄奐暊偟丄墿懱悢丄惗懚偍傛傃巰朣戀巈悢傪挷傋丄桪惈抳巰桿敪棪傪媮傔偨丅桪惈抳巰桿敪棪偼壓婰偺俀捠傝乮俙丆俛乯偺幃偵傛傝嶼弌偟偨丅
丂俙亖乵侾亅乮擠怭帗偁偨傝偺惗懚戀巈悢丗張棟孮乛擠怭帗偁偨傝偺惗懚戀巈悢丗懳徠孮乯乶亊侾侽侽
丂俛亖乵侾亅乮擠怭帗偁偨傝偺惗懚戀巈悢乛拝彴悢丗張棟孮乯丂亐丂乮擠怭帗偁偨傝偺惗懚戀巈悢乛拝彴悢丗懳徠孮乯乶亊侾侽侽
丂傑偨梲惈懳徠孮埲奜偺孮偵偍偄偰張棟婜娫拞丄廡偵侾搙懱廳偍傛傃愛塧検傪應掕偟偨丅
丂懱廳偍傛傃愛塧検偼搳梌婜娫傪捠偠偰丄懡偔偺応崌丄堿惈懳徠孮傪偆傢傑傢偭偰偄偨丅
丂昞俙亅俆偵偦傟偧傟偺孮偺暯嬒墿懱悢丄拝彴悢丄惗懚戀巈悢丄側傜傃偵桿敪桪惈抳巰棪傪帵偡丅旕徠幩偍傛傃徠幩偺僂僀儞僫乕僜乕僙乕僕孮偺偡傋偰偵偍偄偰丄桿敪桪惈抳巰棪偼晧偺抣傪帵偟偨丅偙偺偙偲偼堿惈懳徠孮偺拝彴悢偺彮側偐偭偨偙偲偲丄忋偵偺傋偨條偵幚尡孮偱偺懱廳偍傛傃愛塧検偑堿惈懳徠孮傛傝傎偲傫偳偺応崌摑寁揑偵桳堄偵崅偄偙偲傪婲場偡傞傕偺偲巚傢傟偨丅傑偨僂僀儞僫乕偺旕徠幩丄徠幩孮娫偵偍偄偰桳堄側嵎偼擣傔傜傟偢丄偙傟傜偺寢壥偐傜僂僀儞僫乕偺俠倧亅俇侽偵傛傞徠幩偵傛偭偰桪惈抳巰桿敪嶌梡傪桳偡傞暔幙偺惗惉側偳偼婲偙偝側偄傕偺偲寢榑偝傟偨丅