昞 1. 堚揱撆惈帋尡偺庬椶偲帋尡嵽椏
 |
3. 徠幩偲帋尡忦審側偳
丂(1) 僞儅僱僊
丂(2) 僐儊
丂(3) 僐儉僊
丂(4) 僂僀儞僫乕僜乕僙乕僕偍傛傃偐傑傏偙
丂(5) 儈僇儞
丂(6) 僕儍僈僀儌
丂(7) 徠幩僐儉僊暡偵傛傞攞悢惈嵶朎桿敪
丂(8) 徠幩僗僷僀僗偺曄堎尨惈
4. 幚尡寢壥偲峫嶡
丂(1) 僞儅僱僊
丂(2) 僐儊
丂(3) 僐儉僊
丂(4) 僂僀儞僫乕僜乕僙乕僕偍傛傃偐傑傏偙
丂(5) 儈僇儞
丂(6) 僕儍僈僀儌
丂(7) 徠幩僐儉僊暡偵傛傞攞悢惈嵶朎桿敪
丂(8) 徠幩僗僷僀僗偺曄堎尨惈
丂傢偑崙偱徠幩怘昳偺寬慡惈 / 埨慡惈側偳偺憤崌揑側尋媶偑奐巒偝傟偨偺偼丄1967 擭偵堦楢偺尋媶偑尨巕椡摿掕憤崌尋媶偵巜掕偝傟偰偐傜偱偁傞丅偙偺尋媶斍偱偼丄嶦嬠丄嶦拵丄敪夎杊巭側偳偺栚揑偱曻幩慄徠幩偝傟偨怘昳偵娭偟偰丄崙棫帋尡尋媶婡娭 乮摉帪偺塰梴尋媶強丄梊杊塹惗尋媶強丄塹惗帋尡強乯 偑拞怱偲側傝丄塰梴惉暘偺曄壔丄枬惈撆惈帋尡丄悽戙帋尡側偳偺帋尡偑僗僞乕僩偟偨丅偦偺屻丄敪偑傫傗師悽戙偱偺堚揱揑忈奞偺梊抦偵偐偐傢傞堚揱撆惈偺廳梫惈偑堦斒偵擣幆偝傟巒傔傞傛偆偵側偭偨偺偼 1970 擭戙偵擖偭偰偐傜偱偁傞丅恅栰尋媶強偱偼丄1977 擭傛傝徠幩怘昳偵娭偟偰嵶嬠丄攟梴嵶朎丄摦暔屄懱傪梡偄偨憤崌揑側堚揱撆惈帋尡傪奐巒偟偨1)丅偦偺拞偵偼丄尰嵼偱偼懡悢偺摦暔傪梡偄傞偙偲偐傜摦暔垽岇偺娤揰傛傝幚巤偑擄偟偄師悽戙 乮惗怋嵶朎傊偺塭嬁乯 傊偺堚揱撆惈傪挷傋傞桪惈抳巰帋尡偲偄偭偨戝婯柾側帋尡傕娷傑傟偰偄傞丅徠幩怘昳偵傛傞堚揱妛揑塭嬁偵娭偟偰丄偙偺傛偆側懡庬偺帋尡宯傪梡偄偨僶僀僆傾僢僙僀偵傛傞憤崌揑側尋媶偼崙嵺揑偵傕椺傪尒側偄偙偲偐傜丄偄偔偮偐偺尋媶斍曬崘彂傪傑偲傔偙偙偵徯夘偡傞丅
丂偙偙偱帋尡偝傟偨怘昳偦偺傕偺偼丄捠忢変乆偑怘偟偰偄傞擾嶻暔偍傛傃怘擏壛岺怘昳偱偁傝丄挿偄怘宱尡偐傜怘昳偲偟偰偼宱尡揑偵埨慡惈偑妋擣偝傟偰偄傞傕偺偱偁傞丅堚揱揑埨慡惈傪挷傋傞偵偼丄懳徠偲偟偰梡偄傞旕徠幩怘昳偺撆惈斀墳偲偺斾妑偵側傞偑丄旕徠幩偺怘昳偦偺傕偺偵偍偄偰傕摦暔傪梡偄偨撆惈帋尡偺幚巤偼丄搳梌検丄怘昳偺宍懺丄搳梌宱楬丄塰梴揑側僶儔儞僗側偳偱條乆側崲擄偑敽偆丅堚揱撆惈帋尡偱偼丄曻幩慄徠幩偵敽偭偰惗偠傞偐傕偟傟側偄怘昳拞偺曻幩慄暘夝惗惉暔偵傛傞堚揱揑側桳奞惈偺壜擻惈偵偮偄偰専摙偡傞帠偵側傞丅
丂堚揱撆惈偲偼丄岺嬈尨椏丄堛栻丄擾栻丄娐嫬墭愼暔幙側偳偺壔妛暔幙傗丄曻幩慄丄巼奜慄側偳暔棟壔妛揑側梫場偵傛傝 DNA 側偳偵彎奞傪梌偊堚揱宍幙傪曄壔偝偣傞帠徾偱丄DNA 懝彎丄撍慠曄堎丄愼怓懱堎忢傑偱傪曪娷偡傞 乮拲 : 曄堎尨惈 (Mutagenicity) 偺梡岅偑堦斒偵梡偄傜傟偰偒偨偑丄嬤擭丄崙嵺揑偵傑偨峴惌偺僈僀僪儔僀儞偵偍偄偰傕峀媊偺堄枴偱堚揱撆惈 乮Genotoxicity乯 偑巊傢傟偰偄傞乯丅昗揑偼庡偲偟偰 DNA 偱偁傞偑丄DNA 偵尷傜偢僞儞僷僋側偳偑廋忺偝傟傞帠偵傛傝丄寢壥偲偟偰愼怓懱偺愗抐傗嵞寢崌丄悢揑堎忢側偳傪惗偠傞応崌傕偁傞丅偙偺傛偆側 DNA 傗愼怓懱偺彎奞偼丄懱嵶朎偱偼偑傫偺桿敪梫場偲側傝丄惗怋嵶朎偱惗偠偦傟偑庴惛偵偁偢偐傞偲泱巰朣傗棳嶻丄婏宍丄偦偟偰揮嵗傗堚揱巕堎忢傪桳偡傞屄懱傪弌嶻偡傞壜擻惈偑偁傞丅
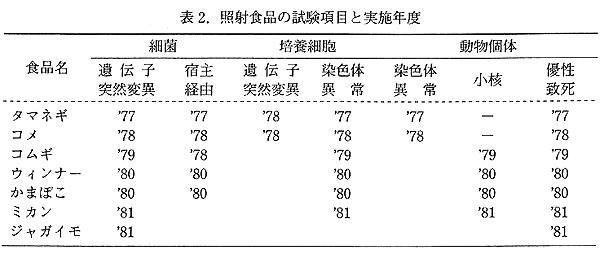
丂堚揱撆惈偺専弌偼偦偺僄儞僪億僀儞僩偵傛傝帋尡宯偼條乆偱偁傞丅昞 1 偵帋尡偺庬椶偲嵶朎側偳偺嵽椏傪帵偟偨丅1977 擭偐傜 1981 擭偵偐偗偰尨巕椡摿掕憤崌尋媶偱帋尡偝傟偨怘昳偼丄僞儅僱僊丄僐儊丄僐儉僊丄僂僀儞僫乕僜乕僙乕僕丄偐傑傏偙丄儈僇儞丄僕儍僈僀儌偺 7 昳栚偱丄昞 2 偵帋尡崁栚偲幚巤擭搙傪帵偟偨丅
丂捠忢丄嵶嬠傗嵶朎傪梡偄傞堚揱巕撍慠曄堎帋尡偲偟偰偼丄嵶嬠傪梡偄傞暅婣曄堎帋尡傗 V79 嵶朎傗儅僂僗儕儞僼僅乕儅嵶朎傪梡偄傞栻嵻掞峈惈傪儅乕僇乕偲偡傞帋尡偑偁傞偑丄徠幩怘昳偱偼嵶嬠傪梡偄傞暅婣曄堎帋尡偲 V79 嵶朎傪梡偄傞帋尡偑幚巤偝傟偨丅惗懱撪偱戙幱偝傟曄堎尨惈傪帵偡暔幙偺専弌偵娭偟偰偼丄嵟嬤偼栻暔桿摫傪偐偗偨儔僢僩娞憻偐傜摼傜傟偨娞儂儌僕僱乕僩傪梡偄傞戙幱妶惈壔帋尡偑幚巤偝傟偰偄傞偑丄摉帪偼廻庡宱桼朄傕峴傢傟偨丅偙偺帋尡偼専懱傪儅僂僗偵搳梌偟丄偦偺屻暊峯撪偵帋尡嬠姅傪抁帪娫拲擖偟偰夞廂偟丄偦偺撍慠曄堎傪挷傋傞曽朄偱偁傞丅攟梴嵶朎傪梡偄傞帋尡偲偟偰偼丄V79 嵶朎傪梡偄傞堚揱巕撍慠曄堎帋尡丄僠儍僀僯乕僘丒僴儉僗僞乕嵶朎傗僸僩儕儞僷媴傪梡偄傞愼怓懱堎忢帋尡偑峴傢傟偨丅摦暔屄懱傪梡偄傞帋尡偲偟偰偼丄儅僂僗偍傛傃僠儍僀僯乕僘丒僴儉僗僞乕側偳偺摦暔傪梡偄偰愼怓懱堎忢帋尡丄彫妀帋尡丄桪惈抳巰帋尡側偳偑幚巤偝傟偨丅桪惈抳巰帋尡偱偼丄奺孮 30 摢偺梇儅僂僗傪梡偄丄枅廡 1 摢偺梇偵懳偟 2 摢偺帗儅僂僗偲岎攝偟偙傟傪 8 廡娫懕偗傞偲丄寁嶼忋 480 摢偺擠怭帗儅僂僗偑摼傜傟傞丅1 帋尡偱 1 旕徠幩孮丄2 徠幩孮丄1 梟攠懳徠孮丄1 梲惈懳徠孮偺慡 5 孮峔惉偱偁傞偙偲偐傜丄(30 + 480)亊5 孮偱 2550 摢偺儅僂僗傪梡偄偨偙偲偵側傞丅杮尋媶偱偼丄忋婰偺帋尡忦審偱幚巤偡傞僼儖桪惈抳巰帋尡偲丄専懱傪挿婜張棟偟岎攝傪 1 廡娫偺傒幚巤偡傞娙曋朄偺擇偮偺曽朄偱幚巤偟偨 乮昞 3乯丅
丂僞儅僱僊丄儈僇儞丄僕儍僈僀儌丄僐儉僊暡偺桪惈抳巰帋尡偱偼 8 廡娫楢懕岎攝偺僼儖僥僗僩傪幚巤偟偨丅8 廡娫傕偺挿婜偵傢偨偭偰岎攝偡傞棟桼偼丄儅僂僗偺応崌丄惛巕偺姴嵶朎 乮stem cell乯 偱偁傞惛慶嵶朎偐傜惛巕偵側傞傑偱偺惛巕宍惉夁掱 乮spermatogenesis乯 偼偍傛偦 6 廡娫偐偐傞偙偲偐傜丄徠幩怘昳偺塭嬁傪惛巕暘壔偺慡夁掱偲姴嵶朎偲側傞惛慶嵶朎偺憹怋婜偵傕嶌梡偝偣偰挷傋傞堊偵挿婜偵傢偨偭偰岎攝偟偨丅儅僂僗偼恅栰尋媶強偱忢偵巊梡偟丄攚宨僨乕僞偺偁傞 BDF1 儅僂僗 乮C57BL 偲 DBA 偺嬤岎宯娫岎攝 F1 儅僂僗乯 傪梡偄偨丅
丂尨巕椡摿掕憤崌尋媶偑廔椆偟偨屻丄1986 擭偐傜 1991 擭偵偐偗偰丄擔杮傾僀僜僩乕僾嫤夛丒怘昳徠幩埾堳夛偱偼丄摉帪崙嵺揑偵榑揰偲側偭偰偄偨婔偮偐偺尋媶偵娭偟偰帋尡傪峴偭偨丅僀儞僪偱曬崘2, 3) 偝傟偨攞悢惈嵶朎偺桿敪傪妋擣偡傞偨傔丄僈儞儅慄徠幩偟偨彫敒暡傪僠儍僀僯乕僘丒僴儉僗僞乕偲儔僢僩偵媼塧偟崪悜嵶朎偱偺攞悢惈嵶朎桿敪偲枛徑寣愒寣媴偱偺彫妀桿敪傪傒傞帋尡傪幚巤偟偨丅傑偨丄嵶嬠側偳偺墭愼偑懡偄僗僷僀僗偵娭偟偰偼丄僈儞儅慄徠幩偵傛傞僗僷僀僗偺撍慠曄堎桿敪傪嵶嬠傪梡偄傞暅婣曄堎帋尡傪梡偄偰専摙偟偨丅
 |
 |
 |
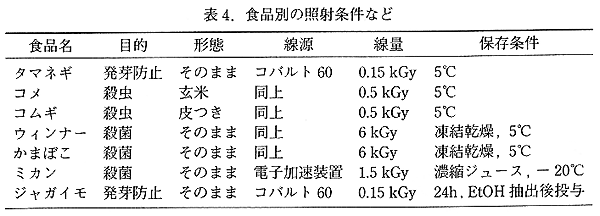
丂帋尡偟偨怘昳偺徠幩栚揑偲徠幩帪偺帋椏偺忬懺丄徠幩慄検側偳偺帋尡忦審傪昞4偵帵偟偨丅慄尮偼儈僇儞偺揹巕慄徠幩傪彍偒丄偡傋偰僐僶儖僩 60 偵傛傞兞慄徠幩偵傛偭偨丅
 |
丂僞儅僱僊偼敪夎杊巭偺栚揑偱偁傞偑丄幚梡忋尷偺慄検偱偁傞 0.15kGy 偱徠幩屻丄5 儢寧娫丄5亷 偺椻埫強偱挋憼偟偨傕偺傪梡偄偨丅
丂嵶嬠傪梡偄傞暅婣曄堎帋尡媦傃廻庡宱桼帋尡偱偼 TA1535丄TA100丄TA1537丄TA98 偺嬠姅傪梡偄偨丅徠幩僞儅僱僊偺帋椏偼僞儅僱僊傪儈僉僒乕偱僕儏乕僗偵偟偰傠夁偟偨屻丄尭埑擹弅偟丄-20亷 壓偱搥寢曐懚偟偨丅in vitro 愼怓懱堎忢帋尡偱偼摨條偵偟偰嶌惢偟偨搥寢姡憞暡枛傪梡偄偨丅in vivo 偺帋尡偵偍偄偰傕丄帋椏傪壠掚梡偺僕儏乕僒乕丄偝傜偵儂儌僽儗儞僟乕偱暡嵱偟丄偙偺儂儌僕僱乕僩傪搥寢姡憞偟偰帋椏偲偟偨丅
丂9 廡楊 BDF1 梇儅僂僗傪梡偄傞愼怓懱堎忢帋尡偲桪惈抳巰帋尡偱偼丄搳梌偼搥寢姡憞帋椏偵忲棷悈傪壛偊偰崿榓偟丄徠幩僞儅僱僊搳梌孮偱偼 1 擔偁偨傝 2 g/kg (愼怓懱堎忢帋尡偺傒)丄4 g/kg丄偍傛傃 8 g/kg丄旕徠幩僞儅僱僊搳梌孮偱偼 8 g/kg丄堿惈懳徠偱偼忲棷悈傪丄5 擔娫丄堓僝儞僨傪梡偄偰楢懕搳梌偟偨丅梲惈懳徠偼 MMS 乮儊僠儖儊僞儞僗儖僼僅僱乕僩乯丄100 mg/kg 傪 1 夞暊峯搳梌偟偨丅愼怓懱堎忢帋尡偱偼奺孮 5 摢偺梇儅僂僗傪梡偄丄嵟廔搳梌偺 20 帪娫屻偵崪悜嵶朎偺愼怓懱昗杮傪嶌惉偟偨丅桪惈抳巰帋尡偱偼奺孮 15 - 19 摢偺梇儅僂僗傪梡偄丄嵟廔搳梌屻 8 廡偵傢偨傝丄枅廡 1 摢偺梇儅僂僗偁偨傝 2 摢偺帗儅僂僗偲岎攝偟偨丅岎旜妋擣屻丄帗儅僂僗偼擠怭 13 擔偵夝朥偡傞傑偱暿働乕僕偱帞堢偟偨丅擠怭 13 擔栚偵夝朥偟偰墿懱悢 乮攔棏悢偺悇掕乯 傗拝彴悢丄惗懚泱丄巰泱側偳傪挷傋偨丅
丂僐儊偺徠幩偼嶦拵偺栚揑偱偁傞丅尯暷傪幚梡忋尷偺慄検偱偁傞 0.5 kGy 徠幩偟偨丅嵶嬠傪梡偄傞暅婣曄堎帋尡偱偼 TA100 偍傛傃 TA98 偺嬠姅傪梡偄偨丅偙傟傜偺嬠姅偱偼僸僗僠僕儞梫媮惈偐傜旕梫媮惈傊偺暅婣曄堎傪巜昗偲偟偰挷傋傞偨傔丄僸僗僠僕儞傪娷桳偡傞帋椏偱偺帋尡偼栤戣偑偁傞偙偲偐傜丄帋尡偵梡偄偨 80% 儊僞僲乕儖拪弌塼偺尭埑擹弅暔偵偮偄偰傾儈僲巁暘愅傪偟偨丅偦偺寢壥 100g 偺尯暷偁偨傝偺傾儈僲巁偺慡検偼 4.275g丄偦偺偆偪僸僗僠僕儞偼 0.06mg 偲旕忢偵彮側偄検偱偁偭偨偙偲偐傜偦偺塭嬁偼側偄偲敾抐偟偨丅
丂廻庡宱桼帋尡偱偼丄1 孮 5 摢偺儅僂僗傪梡偄丄1 擔 1 夞丄忋婰偺帋椏 0.5mL 傪 3 擔娫楢懕宱岥搳梌偟偨丅3 夞栚偺搳梌偲摨帪偵専掕嬠塼 1mL 傪暊峯撪偵搳梌偟丄3帪娫屻偵寊捙扙塒屻丄惗棟怘墫悈 1mL 傪暊峯撪偵搳梌偟偰暊峯撪偺専掕嬠塼傪夞廂偟偰撍慠曄堎傪挷傋偨丅V79 嵶朎傪梡偄傞撍慠曄堎帋尡偱偼丄100% 傑偨偼 80% 偺儊僞僲乕儖丄傑偨偼悈偱拪弌偟偨傕偺傪尭埑擹弅偟偰帋椏尨塼偲偟偨丅偙傟傜偺帋椏傪嵶朎偵 16 帪娫嶌梡偝偣丄144 帪娫偺敪尰帪娫偱撍慠曄堎偺桿敪傪挷傋偨丅 in vitro 愼怓懱堎忢帋尡偱偼 CHL/IU 嵶朎傪梡偄偨丅80% 儊僞僲乕儖傪梡偄偰拪弌偟偨尯暷僄僉僗傪庬乆偺擹搙偱丄24 媦傃 48 帪娫張棟偟偰昗杮嶌惢偟偨丅僠儍僀僯乕僘丒僴儉僗僞乕傪梡偄傞媫惈偺 in vivo 愼怓懱堎忢帋尡偱偼丄1 孮 5 摢 (8 廡楊丄暯嬒懱廳 33g丄梇) 偺摦暔傪梡偄丄徠幩暷偺崅梡検搳梌孮偱偼僐儊暡枛 1g 傪悈 1.5 ml丄掅梡検孮偱偼 1g 傪悈 3ml 偵寽戺偟摦暔懱廳 乮g乯 偁偨傝 0.05 mL 傪堓僝儞僨傪梡偄偰宱岥揑偵 1 夞搳梌偟偨丅堦曽丄崿塧搳梌偺帋尡偱偼丄徠幩暷傪 40% 娷桳偡傞屌宍塧椏傪 5 擔娫帺桼偵愛怘偝偣偨丅
丂儅僂僗傪梡偄傞桪惈抳巰帋尡偱偼丄1 孮 30 摢偺梇儅僂僗傪梡偄丄徠幩暷 40% 娷桳屌宍塧椏傪 6 廡楊偐傜 14 廡楊傑偱偺 8 廡偵傢偨傝愛怘偝偣偨丅岎攝偼丄搳梌屻 1 廡娫偺姶庴惈偺崅偄帪婜偵丄1 摢偺梇偵懳偟偰 2 摢偺帗儅僂僗偲岎攝偟偨丅
丂暷崙嶻 乮Dark Northern Spring乯 偺僐儉僊偵丄幚梡忋尷偺慄検偱偁傞 0.5 kGy 傪徠幩偟帋椏傪嶌惢偟偨丅嵶嬠傪梡偄傞撍慠曄堎桿敪帋尡偱偼僐儉僊傪 70% 儊僞僲乕儖偵 100mg/mL 偺妱崌偵晜梀偝偣丄幒壏偵4帪娫曻抲屻帋尡偵梡偄偨丅愼怓懱堎忢帋尡偲廻庡宱桼帋尡偱偼丄僐儉僊 2kg 傪 6L 偺 70% 偺儊僞僲乕儖偱拪弌偟丄尭埑擹弅屻丄搥寢姡憞偟偨傕偺傪梡偄偨 乮徠幩僐儉僊 1kg 摉傝偺搥寢姡憞暔廳検偼 58.2g 偱偁傞乯丅
丂摦暔傪梡偄傞愼怓懱堎忢帋尡偱偼丄儅僂僗傪梡偄傞彫妀帋尡傪戙懼帋尡偲偟偰幚巤偟偨丅帋椏偼徠幩僐儉僊拪弌暔傪 0.5% CMC-Na 塼偵寽戺偟丄儅僂僗懱廳偁偨傝偦傟偧傟 72.5丄145丄290mg/kg 傪 1 擔 1 夞丄5 擔娫偵傢偨偭偰宱岥搳梌偟偨丅旕徠幩僐儉僊偼 283mg/kg丄梲惈懳徠偼 MTX 乮儊僜僩儗僉僙乕僩乯丄2.5mg/kg 傪偦傟偧傟 5 擔娫楢搳偟偨丅桪惈抳巰帋尡偱偼丄僐儊偺応崌偲摨條偵崿塧偵傛傝 8 廡娫愛怘偝偣丄娙曋朄偵傛傝搳梌屻 1 廡娫岎攝偟偨丅
丂僂僀儞僫乕僜乕僙乕僕偍傛傃偐傑傏偙偼偦偺傑傑偺忬懺偱幚梡慄検忋尷偺栺 2 攞偵偁偨傞 6kGy 徠幩偟丄搥寢姡憞偟偨傕偺傪慡偰偺帋尡偵梡偄偨丅in vitro 愼怓懱堎忢帋尡偱偼搥寢姡憞暔偺儊僞僲乕儖拪弌暔傪僸僩儕儞僷媴偍傛傃僠儍僀僯乕僘丒僴儉僗僞乕嵶朎偵張棟偟偨丅in vivo 偱偺儅僂僗崪悜嵶朎偺彫妀帋尡偲桪惈抳巰帋尡偱偼丄搥寢姡憞暔傪梡偄偰娙曋朄偵傛傝帋尡偟偨丅
丂儈僇儞偼 1.5kGy 偱揹巕慄柵嬠偟丄擹弅僕儏乕僗 (5 攞) 偺忬懺偱 -20亷 偵曐懚偟帋尡偵梡偄偨丅嵶嬠傪梡偄傞帋尡偱偼丄擹弅僕儏乕僗傪暯斅摉傝丄0.5mL 偍傛傃 1.0mL 揧壛偟偰帋尡偵梡偄偨丅儅僂僗彫妀帋尡偱偼丄奺孮 5 摢偺儅僂僗偵擹弅僕儏乕僗傪 1 擔 2 夞丄5 擔娫宱岥搳梌偟丄嵟廔搳梌偺 20 帪娫屻偵彫妀昗杮傪嶌惢偟偨丅桪惈抳巰帋尡偱偼 1 孮 30 旵偺梇儅僂僗偵擹弅僕儏乕僗傪 1 擔 2 夞丄5 擔娫宱岥搳梌偟丄偦偺屻 4 擔偵 1 夞丄8 廡娫偵傢偨傝 1 摢偺帗儅僂僗偲岎攝偟偨丅
丂僕儍僈僀儌偼僄僞僲乕儖拪弌暔傪梡偄偰奺帋尡傪幚巤偟偨丅僕儍僈僀儌偼丄傢偑崙偵偍偄偰敪夎杊巭偺栚揑偱 0.15kGy 埲壓偺兞慄徠幩偑嫋壜偝傟偨桞堦偺怘昳偱偁傞丅1972 擭丄Kuzin 傜4) 偵傛傝徠幩僕儍僈僀儌偺僄僞僲乕儖拪弌暔偑儅僂僗偵偍偄偰桪惈抳巰傪桿敪偡傞偲偺曬崘偑側偝傟偨帠偐傜丄徠幩忦審摍偼偦偺榑暥偵崌傢偣丄徠幩 24 帪娫屻僄僞僲乕儖拪弌偟丄拪弌暔傪 1 擔 2 夞丄7 擔娫宱岥搳梌偟偨丅偦偺屻丄4 擔偵 1 夞丄偦傟偧傟 1 摢偺帗儅僂僗偲岎攝偟丄搳梌屻 8 廡娫偵傢偨傝岎攝傪懕偗偨丅奺孮 30 摢偺梇儅僂僗傪梡偄偨丅
丂徠幩僐儉僊暡傪摦暔偵挿婜娫梌偊傞偲攞悢惈嵶朎傪桿敪偡傞偲偄偆 Renner5) 偺曬崘丄傑偨塰梴幐挷偺巕嫙偵徠幩僐儉僊傪梌偊傞偲攞悢惈嵶朎偑崅偔側傞偲偄偆 Bhaskaram 傜偺曬崘6) 偑偁傞偙偲偐傜丄徠幩僐儉僊暡傪徠幩捈屻偵媼塧偟偨応崌偲丄挿婜娫媼塧偟偨応崌偺嵶朎堚揱揑塭嬁偵偮偄偰丄僠儍僀僯乕僘丒僴儉僗僞乕偲儔僢僩傪梡偄偰挷傋偨丅
丂僠儍僀僯乕僘丒僴儉僗僞乕傪梡偄傞幚尡偱偼丄徠幩僐儉僊暡偺徠幩忦審偼 Renner 偺徠幩柵嬠帞椏偺忦審偵嬤偄丄7.5kGy丄15kGy丄30kGy 傪徠幩偟偨丅徠幩帪偺儔僕僇儖嶻惗偵傛傞塭嬁傪尒傞偨傔傪丄扙婥偟偰拏慺僈僗偵抲姺偟偨孮偲抲姺偟側偄孮傪愝偗偨丅僴儉僗僞乕傊偺媼塧偼丄奺孮 6 摢偺僴儉僗僞乕偵丄徠幩 8 帪娫屻偵暡枛帞椏偲偟偰 8 - 72 帪娫埲撪偵梌偊偨丅媼塧奐巒 72 帪娫屻偵昗杮嶌惢偟崪悜嵶朎偺攞悢惈嵶朎偺暘愅偵梡偄偨丅傑偨丄48 帪娫屻偍傛傃 72 帪娫屻偺枛徑寣傪旜晹偐傜嵦寣偟丄椦傜偺曽朄7) 偵傛傝枛徑愒寣媴偺彫妀昗杮傪嶌惢偟偨丅愼怓偼傾僋儕僕儞僆儗儞僕愼怓偵傛偭偨丅
丂儔僢僩傪梡偄傞幚尡偱偼丄僐儉僊暡偺徠幩偼 Vijayalaxmi 傜2) 偺慄検偵偁傢偣丄0.75kGy 偲偟偨丅徠幩僐儉僊偼徠幩 2 擔屻偵暡枛帞椏偲偟偰丄奺孮 9 摢偺儔僢僩偵 6 廡娫偍傛傃 12 廡娫媼塧偟丄偦偺屻崪悜嵶朎偐傜愼怓懱昗杮傪嶌惢偟偨丅枛徑寣偐傜偼彫妀昗杮傪嶌惢偟偨丅
丂帋尡偼丄TA100丄TA98 偍傛傃 TA102 偺 3 嬠姅傪梡偄傞暅婣曄堎帋尡傪幚巤偟偨丅僗僷僀僗偼崟僐僔儑僂丄愒僩僂僈儔僔丄僫僣儊僌丄僷僾儕僇傪梡偄偨丅徠幩慄検偼 1kGy 偲 10kGy 偱徠幩偟丄挻椪奅棳懱拪弌偵傛傝拪弌暔傪嶌惉偟偨丅崟僐僔儑僂偵偮偄偰偼丄50% 拪弌暔傕暪偣偰嶌惢偟偨丅
丂尨巕椡摿掕憤崌尋媶偱幚巤偟偨 7 昳栚偺徠幩怘昳偵偮偄偰偺堚揱撆惈帋尡寢壥傪昞 5 偵帵偟偨丅帋尡偟偨慡偰偺徠幩怘昳偵偍偄偰丄偳偺帋尡宯偵偍偄偰傕慡偰堿惈偺寢壥偑摼傜傟偨丅偦傟偧傟偺僨乕僞偵偮偄偰弎傋傞丅
 |
丂嵶嬠傪梡偄傞暅婣曄堎帋尡偱偼丄帋尡偵梡偄偨 4 嬠姅慡偰偵偍偄偰丄徠幩丄旕徠幩偲傕偵丄傑偨戙幱妶惈壔偺桳柍偵尷傜偢丄曄堎僐儘僯乕偺憹壛偼尒傜傟側偐偭偨丅傑偨丄廻庡宱桼帋尡偵偍偄偰傕丄摨條偵慡偰偺梡検偵偍偄偰懳徠孮偲偺嵎偼尒傜傟偢丄嵶嬠傪梡偄傞宯偱偼徠幩僞儅僱僊偺曄堎尨惈偼擣傔傜傟側偄偲敾抐偟偨丅
丂攟梴嵶朎傪梡偄傞愼怓懱堎忢帋尡偱偼丄僸僩戀帣桼棃嵶朎 乮HE2144乯 偲僠儍僀僯乕僘丒僴儉僗僞乕桼棃 乮Don-6乯 嵶朎傪梡偄偰丄愼怓懱堎忢偲 SCE 媦傃彫妀偺桿敪偑挷傋傜傟偨丅偦偺寢壥丄徠幩僞儅僱僊僄僉僗偺搥寢暡枛偼丄僸僩嵶朎偵懳偟偰徠幩偍傛傃旕徠幩孮偲傕偵 2mg/ml 偱挊偟偄暘楐梷惂偑尒傜傟偨丅僴儉僗僞乕嵶朎偱偼丄徠幩孮偱偼 4mg/ml丄旕徠幩孮偱偼 2mg/ml 偱摨條偺暘楐梷惂偑尒傜傟偨丅愼怓懱愗抐偵娭偟偰偼丄僠儍僀僯乕僘丒僴儉僗僞乕偱偼愼怓懱愗抐偺憹壛偑尒傜傟偨偑丄徠幩孮傛傝傓偟傠旕徠幩孮偱傗傗崅偔堎忢偑桿敪偝傟偨丅僸僩嵶朎偱偼杦傫偳塭嬁偑側偐偭偨丅彫妀偺桿敪偵娭偟偰傕摨條側孹岦偑尒傜傟偨偑丄徠幩偵傛傞嵎偼傒傜傟側偐偭偨丅SCE 偺桿敪偵娭偟偰偼丄徠幩丄旕徠幩偲傕偵 SCE 偑桿敪偝傟偨偑丄徠幩偵傛傞嵎偼尒傜傟側偐偭偨丅
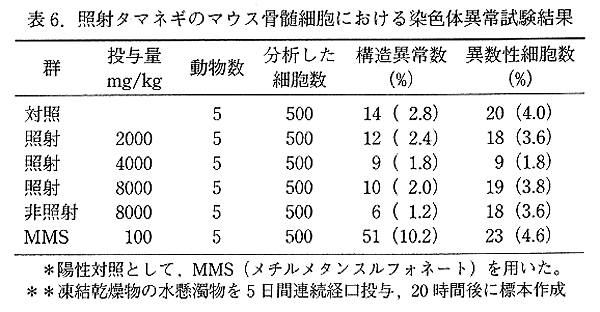
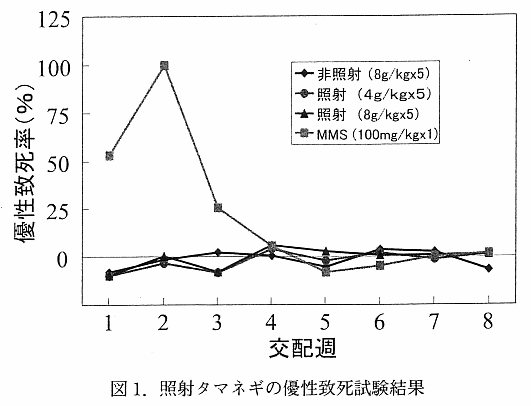
丂儅僂僗 乮BDF1乯 傪梡偄偨 in vivo 愼怓懱堎忢帋尡偺寢壥傪昞 6 偵帵偟偨丅僞儅僱僊偺搥寢姡憞暡枛偵悈偵寽戺偟偨徠幩専懱搳梌偺偄偢傟偺孮偵偍偄偰傕丄懳徠孮偲斾傋偰愼怓懱堎忢偺桳堄側憹壛偼尒傜傟側偐偭偨丅摿偵丄8000mg/kg 傪 5 擔娫楢懕宱岥搳梌 乮懱廳 50kg 偺僸僩偑惗僞儅僱僊 4kg 傪 5 擔娫枅擔怘傋傞検偵憡摉乯 偡傞偲偄偆夁崜側忦審偵偍偄偰傕丄徠幩偵傛傞塭嬁偼傒傜傟側偐偭偨丅堦曽丄儔僢僩 (Long-Evans 宯) 偺崪悜嵶朎傪梡偄偨愼怓懱堎忢帋尡偱偼丄宱岥搳梌偲暊峯撪搳梌偺帋尡傪偍偙側偭偨偑丄偄偢傟偺帋尡偱傕徠幩孮偲旕徠幩孮偱桳堄側堎忢桿敪偼尒傜傟側偐偭偨丅桪惈抳巰帋尡偺寢壥傪恾 1 偵帵偟偨偑丄徠幩偍傛傃旕徠幩偲傕偵丄墿懱悢丄拝彴悢丄惗懚泱悢丄巰泱悢側偳偵丄桳堄側曄壔偼傒傜傟偢丄徠幩偵傛傞桪惈抳巰偺桿敪偼擣傔傜傟側偐偭偨丅
 |
 |
 |
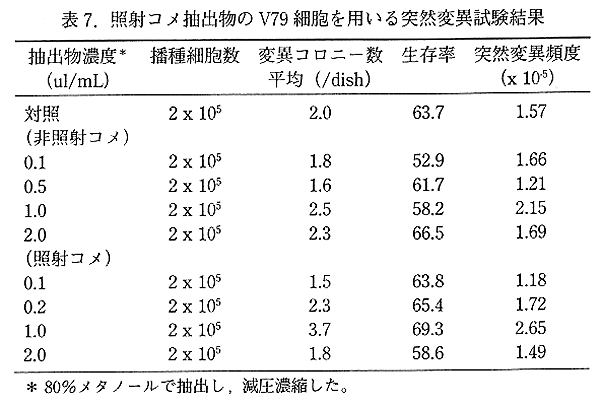
丂嵶嬠傪梡偄傞暅婣曄堎帋尡偱偼丄TA100丄TA98偺椉嬠姅嫟偵徠幩丒旕徠幩傪栤傢偢曄堎僐儘僯乕偺憹壛偼尒傜傟側偐偭偨丅傑偨丄廻庡宱桼帋尡偱傕徠幩丒旕徠幩偵偍偄偰曄堎桿敪偼擣傔傜傟側偐偭偨丅V79 嵶朎傪梡偄傞撍慠曄堎桿敪帋尡偱偼丄100%丄80%丄悈偺 3 庬偺尯暷拪弌暔偵偮偄偰徠幩丄旕徠幩偍傛傃戙幱妶惈壔偺桳柍偵偐偐傢傜偢撍慠曄堎偺桳堄側憹壛偼擣傔傜傟側偐偭偨 乮昞 7乯丅僠儍僀僯乕僘丒僴儉僗僞乕偺 CHL/IU 嵶朎傪梡偄傞愼怓懱堎忢帋尡偱偼丄徠幩丒旕徠幩偺 24 帪娫偍傛傃 48 帪娫張棟偺壗傟偺忦審偵偍偄偰傕丄愼怓懱堎忢偺桿敪偼擣傔傜傟側偐偭偨丅
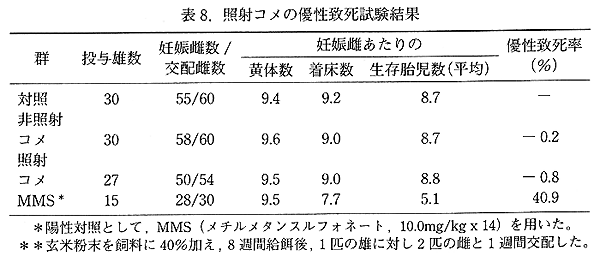
丂僠儍僀僯乕僘丒僴儉僗僞乕偵僐儊暡枛傪堓僝儞僨傪梡偄偰宱岥揑偵 1 夞搳梌偟偨 in vivo 愼怓懱堎忢帋尡偱偼丄崅梡検丄拞梡検孮嫟偵徠幩偍傛傃旕徠幩暷偱偺桳堄側愼怓懱堎忢偺憹壛偼尒傜傟側偐偭偨丅堦曽丄徠幩暷 40% 娷桳偺屌宍塧椏傪 5 擔娫帺桼偵愛怘偝偣偨崿塧搳梌孮偵偍偄偰傕丄桳堄側愼怓懱堎忢桿敪偼擣傔傜傟側偐偭偨丅儅僂僗傪梡偄傞桪惈抳巰帋尡偱偼丄徠幩暷 40% 娷桳屌宍塧椏傪 6 廡楊偐傜 14 廡楊傑偱偺 8 廡偵傢偨傝愛怘偝偣丄搳梌屻 1 廡娫偵 1 摢偺梇偵懳偟偰 2 摢偺帗儅僂僗偲岎攝偟偨寢壥丄徠幩偍傛傃旕徠幩孮偲傕偵墿懱悢丄拝彴悢丄惗懚泱悢丄巰泱悢側偳偵懳徠孮偲嵎偑傒傜傟偢丄徠幩偵傛傞桪惈抳巰偺桿敪偼擣傔傜傟側偐偭偨 乮昞 8乯丅
 |
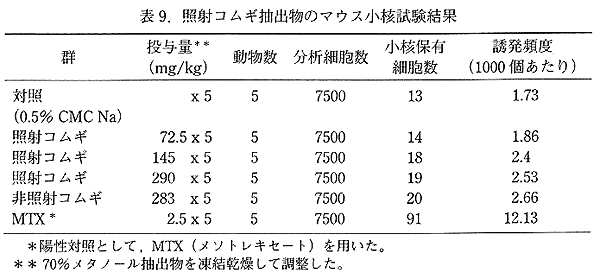
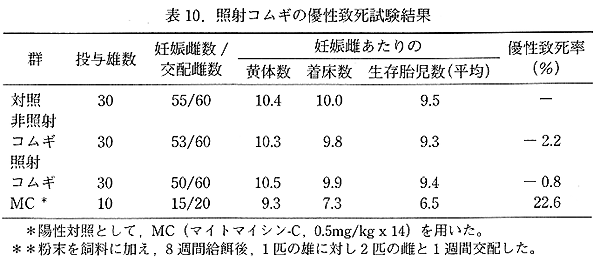
丂嵶嬠傪梡偄傞撍慠曄堎帋尡偱偼丄帋尡偵梡偄偨 6 嬠姅慡偰偵偍偄偰丄徠幩丒旕徠幩傪栤傢偢撍慠曄堎偺桿敪偼傒傜傟側偐偭偨丅儅僂僗廻庡宱桼帋尡偱偼丄1 孮 6 摢偺儅僂僗偵 1% CMC-Na 悈梟塼偵僐儉僊僄僉僗傪寽戺偟偰丄3 擔娫宱岥搳梌偟偨偑丄暊峯撪傛傝夞廂偟偨専掕嬠塼偵偍偄偰徠幩丒旕徠幩偲傕偵曄堎僐儘僯乕偺桿敪偼擣傔傜傟側偐偭偨丅攟梴嵶朎 乮CHL/IU乯 傪梡偄傞愼怓懱堎忢帋尡偱偼丄僐儉僊拪弌暔傪 0.8mg/mL丄1.0mg/mL丄1.5mg/mL 偺 3 擹搙傪 24 帪娫偍傛傃 48 帪娫張棟偟偨偑丄徠幩丒旕徠幩孮偲傕偵愼怓懱堎忢偺桳堄側桿敪偼擣傔傜傟側偐偭偨丅儅僂僗傪梡偄傞彫妀帋尡偱偼僐儉僊拪弌暔傪 72.5mg/kg丄145mg/kg丄290mg/kg 丄5 擔娫宱岥搳梌偟丄崪悜嵶朎偺彫妀傪娤嶡偟偨丅儅僂僗傊偺搳梌検 290mg/kg 偼丄懱廳 50kg 偺僸僩偺応崌丄僐儉僊 250g 偵憡摉偡傞検偱偁傞丅彫妀傪桳偡傞懡愼惈愒寣媴偺弌尰昿搙偼徠幩丄旕徠幩偲傕偵桳堄側忋徃偼擣傔傜傟側偐偭偨 乮昞 9乯丅徠幩僐儉僊傪 40% 娷傓屌宍帞椏傪 8 廡娫梌偊偨徠幩丒旕徠幩孮偵偍偄偰傕桳堄側桪惈抳巰桿敪棪偼擣傔傜傟側偐偭偨 乮昞 10乯丅Bhaskaram 傜6) 偼丄塰梴幐挷偺巕嫙払偵徠幩僐儉僊傪梌偊偨幚尡偱偼丄儕儞僷媴偺攞悢惈嵶朎偑 6 廡栚偵僺乕僋偵側傝丄偦偺尨場偲偟偰丄挋憼偡傞偲暘夝偡傞傛偆側僐儖僸僠儞條偺暔幙偑僈儞儅慄徠幩偵傛傝惗惉偝傟傞壜擻惈傪偁偘偰偄傞丅壖偵偦偺峫偊偑惓偟偄偲壖掕偡傞偲丄彫妀帋尡傗桪惈抳巰帋尡偵偍偄偰傕壗傜偐偺嶌梡偑尒傜傟偰傕椙偄偲峫偊傞偑丄壗傟偺帋尡傕堿惈偺寢壥偲側偭偨丅
 |
 |
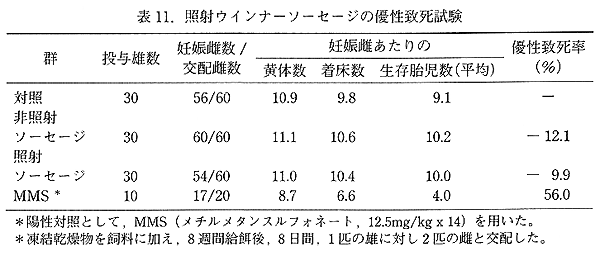
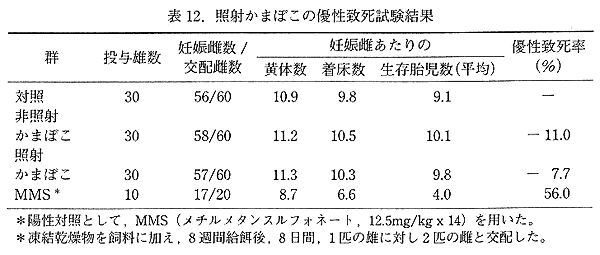
丂僂僀儞僫乕僜乕僙乕僕偍傛傃偐傑傏偙偼幚梡慄検忋尷偺栺 2 攞偵偁偨傞 6kGy 徠幩偟丄儊僞僲乕儖拪弌暔偺搥寢姡憞暔傪摼偨丅嵶嬠傪梡偄傞撍慠曄堎帋尡丄儅僂僗偵傛傞廻庡宱桼帋尡丄僸僩儕儞僷媴偍傛傃僠儍僀僯乕僘丒僴儉僗僞乕嵶朎傪梡偄傞 in vitro 愼怓懱堎忢帋尡偱偼壗傟傕堿惈偺寢壥偑摼傜傟偨丅傑偨丄摦暔傪梡偄偨儅僂僗崪悜嵶朎偺彫妀帋尡偵偍偄偰傕堿惈偲側偭偨丅僂僀儞僫乕僜乕僙乕僕偍傛傃偐傑傏偙偺搥寢姡憞暔傪偦傟偧傟帞椏偵壛偊偰 8 廡娫媼塧偟偨桪惈抳巰帋尡偵偍偄偰偼丄椉帋尡偲傕偵丄徠幩偵傛傞桪惈抳巰偺嶌梡偼擣傔傜傟側偐偭偨 乮昞 11丄12乯丅
 |
 |
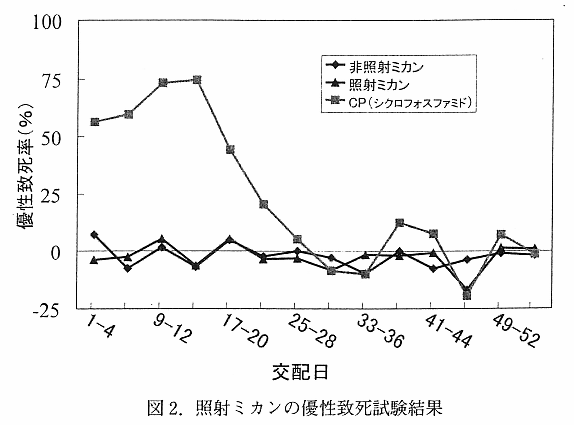
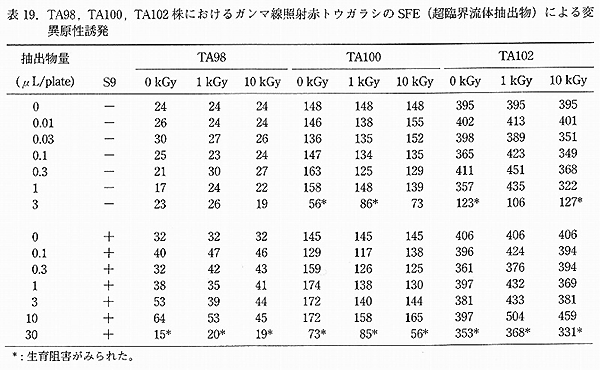
丂嵶嬠傪梡偄傞暅婣曄堎帋尡偱偼 6 嬠姅傪梡偄偨偑丄S9 (-)丄S9 (+) 偺偄偢傟偺忦審壓偵偍偄偰傕曄堎偺桿敪偼擣傔傜傟側偐偭偨丅偨偩偟丄TA100 偵偍偄偰偼徠幩偺桳柍偵偐偐傢傜偢撍慠曄堎棪偑傗傗憹壛 (栺 2 攞掱搙) 偟偨偑丄偙傟偼儈僇儞偵娷傑傟傞偁傞庬偺惉暘偵傛傝曄堎偑桿敪偝傟傞傞偙偲偑抦傜傟偰偄傞偙偲偐傜丄徠幩偵婲場偡傞傕偺偱偼側偄偲敾抐偟偨丅愼怓懱堎忢帋尡偵偍偄偰傕堿惈偲側偭偨丅儅僂僗彫妀帋尡丄桪惈抳巰帋尡偱偼丄儈僇儞擹弅僕儏乕僗 (5 攞) 傪 1 擔 2 夞丄5 擔娫宱岥搳梌偟偨偑丄壗傟偺帋尡偵偍偄偰傕徠幩丒旕徠幩孮偲傕偵桳堄側桿敪偼尒傜傟側偐偭偨 乮恾 2乯丅
 |
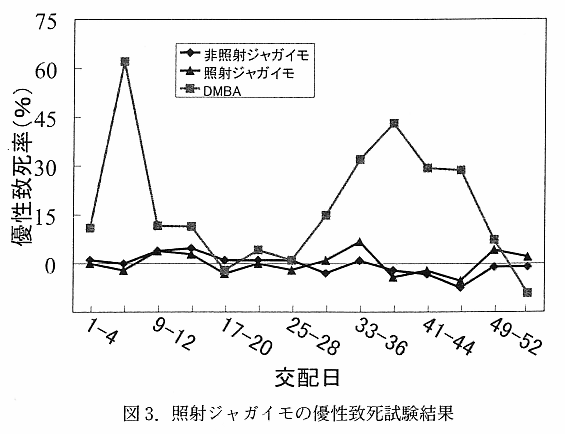
丂幚巤偟偨慡偰偺帋尡偱堿惈偺寢壥偑摼傜傟偨丅徠幩怘昳偺拞偱梲惈偺寢壥偑曬崘偝傟偰偄傞桪惈抳巰帋尡偱偼丄徠幩僕儍僈僀儌偺僄僞僲乕儖拪弌暔偱徠幩丒旕徠幩椉孮嫟偵丄惛巕宍惉夁掱偺慡夁掱偵偍偄偰梲惈偺寢壥傪帵偡傛偆側孹岦偼尒傜傟側偐偭偨 乮恾 3乯丅Kuzin 傜4) 偼丄徠幩僕儍僈僀儌偺僄僞僲乕儖拪弌暔偑儅僂僗偵懳偟偰桪惈抳巰傪桿敪偡傞偲曬崘偟偨丅偙傟偑徠幩怘昳偱堚揱妛揑側婋尟惈傪巜揈偟偨桞堦偺曬崘偱偁傞丅徠幩偵傛傝撆暔 (儔僕僆僩僉僔儞) 偑偱偒傞偨傔偲愢柧偝傟偨偑丄1 孮偁偨傝偺梇儅僂僗傕 5 摢偲彮側偔 乮捠忢偼丄15 乣 30 摢乯丄傑偨丄儅僂僗偺宯摑傕掕偐偱側偄帠偐傜丄帋尡偺嵞尰惈偵栤戣偑偁偭偨帠偑峫偊傜傟傞丅偦偺屻斵傜偼丄壛擬挋憼拞偵儔僕僆僩僉僔儞偼徚柵偡傞帠傪曬崘偟偨丅傑偨丄暘愅壔妛揑側曽朄偱傕専弌偱偒側偐偭偨丅偦偺屻丄IFTA 乮International Project in the Field of Food Irradiation, Karlsruhe, Germany乯 偑僇僫僟偺 Bio-Research Laboratories Ltd. 偵埶棅偟偰峴偭偨帋尡8) 偱傕堿惈偺寢壥偑摼傜傟偰偄傞偑丄偦偺帋尡偵偍偄偰傕 1 孮 5 摢偺梇儅僂僗偟偐梡偄偰側偔丄搳梌屻偺岎攝婜娫偼 5 廡娫偲廫暘側忦審偱偼側偐偭偨丅堦曽丄杮尋媶偱幚巤偟偨桪惈抳巰帋尡偱偼丄摦暔偼忢偵埨掕偟偨寢壥偺摼傜傟傞 BDF1 儅僂僗 乮C57BL 偲 DBA 偺嬤岎宯娫岎攝 F1 儅僂僗乯 傪梡偄丄1 孮 30 摢偺梇偵懳偟丄4 擔偵 1 夞丄楢懕 8 廡娫偺岎攝傪峴偭偰偍傝丄幚尡偺怣棅搙傕嬌傔偰崅偄偲峫偊傞丅埲忋偺寢壥傛傝丄愭偵曬崘偝傟偨梲惈偺曬崘偵娭偡傞嵞尰惈偼摼傜傟偢丄徠幩僕儍僈僀儌偵娭偟偰偼堚揱撆惈偺壜擻惈偼側偄偲寢榑偟偨丅
 |
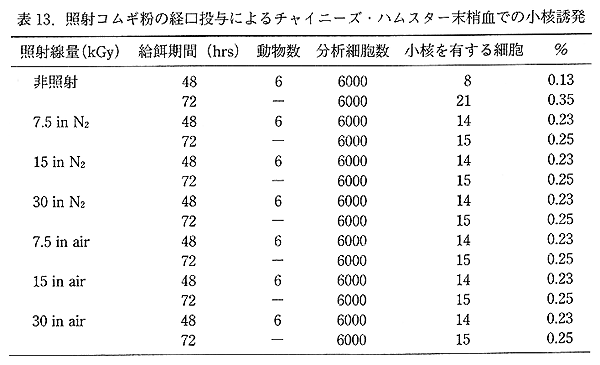
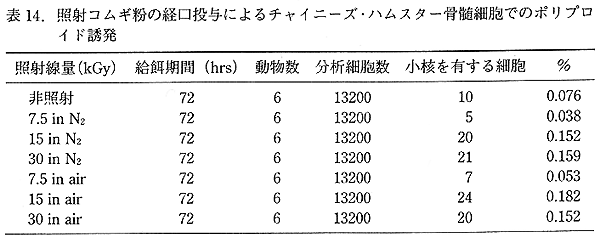
丂徠幩僐儉僊暡偺媼塧奐巒 48 帪娫偍傛傃 72 帪娫屻偺枛徑寣拞偺彫妀暘愅偱偼壗傟偺徠幩孮偵偍偄偰傕彫妀偺桳堄側憹壛偼傒傜傟側偐偭偨丅妶惈巁慺偺惗惉傪梷惂偡傞栚揑偱嬻婥傪拏慺僈僗偵抲姺偟偨孮偲抲姺偟側偄孮偦傟偧傟偵偍偄偰丄旕徠幩孮偲偺娫偱専掕偺孞傝曉偟偵傛傞懡廳惈傪峫椂偟偰 Fischer 偺妋棪寁嶼朄偵傛傝専掕傪峴偭偨寢壥丄偳偺張棟孮偵偍偄偰傕攞悢惈嵶朎偺桳堄側憹壛傗丄慄検埶懚揑側攞悢惈嵶朎偺桿敪偼尒傜傟側偐偭偨9) 乮昞 13丄14乯丅
 |
 |
丂徠幩僐儉僊暡偺媼塧奐巒 6 廡偲 12 廡屻偺枛徑寣拞偺彫妀偵偮偄偰偼丄壗傟偺忦審偵偍偄偰傕桳堄側憹壛偼尒傜傟側偐偭偨丅傑偨丄12 廡屻偺儔僢僩崪悜嵶朎偵偍偗傞攞悢惈嵶朎偵偮偄偰傕旕徠幩孮偲偺娫偵桳堄側憹壛偼尒傜傟側偐偭偨丅
丂杮幚尡偱偼摦暔帞椏偺嶦嬠慄検儗儀儖偱偁傞 30kGy 傪娷傒丄7.5kGy丄15kGy丄30kGy 偺慄検偱徠幩偟偨僐儉僊暡傪丄徠幩 8 帪娫屻偵帞椏偵壛偊偰 3 擔娫僴儉僗僞乕偵媼塧偟偨丅偟偐偟側偑傜丄崪悜嵶朎偵偍偄偰柧傜偐側攞悢惈嵶朎偺桿敪偼尒傜傟側偐偭偨 乮昞 15丄16乯丅傑偨丄杮幚尡偲摨條偵 Tesh 傜 (1977) 傕丄攞悢惈嵶朎偲彫妀桿敪偵娭偟偰徠幩偵傛傞塭嬁偼側偄偙偲傪曬崘10) 偟偰偄傞丅Renner5) 偼丄徠幩屻 3 擔埲撪偵徠幩帞椏傪梌偊偨応崌丄旕徠幩孮偵斾傋偰攞悢惈嵶朎偑憹壛偟丄徠幩 6 廡娫曐懚偟偨屻偵帞椏傪梌偊偨応崌偵偼偦偺塭嬁偑側偄偙偲傪曬崘偟偰偄傞丅偙偺偙偲偼丄徠幩偵傛偭偰儔僕僇儖偑惗惉偝傟丄攞悢惈嵶朎傪桿敪偡傞傛偆側惉暘偺曄壔傪偒偨偟偰偄傞壜擻惈偑帵嵈偝傟偨丅偦偙偱杮幚尡偱偼丄僈儞儅慄徠幩偵傛傞 H2O2 偦偺懠偺妶惈巁慺庬偺惗惉傪梷偊傞栚揑偱丄徠幩帪偺僐儉僊暡拞偺嬻婥傪拏慺偵抲姺偟偨孮偲抲姺偟側偄孮傪愝偗偰幚尡傪峴偭偨丅偟偐偟側偑傜丄壗傟偺忦審壓偵偍偄偰傕攞悢惈嵶朎偺惗惉偵尠挊側嵎偼尒傜傟偢丄攞悢惈嵶朎偵塭嬁傪媦傏偡傛偆側曄壔偼傒傜傟側偐偭偨丅
丂Vijayalaxmi 傜2) 偼丄0.75kGy 偺曻幩慄傪徠幩偟偨僐儉僊傪娷傓帞椏傪儅僂僗丄儔僢僩丄僒儖側偳偵挿婜娫梌偊傞偲攞悢惈嵶朎傪桿敪偡傞偲偄偆曬崘傪偟偰偄傞丅偦偙偱杮幚尡偱偼丄儔僢僩偵 12 廡娫媼塧偟丄崪悜嵶朎偺攞悢惈嵶朎桿敪偲丄枛徑愒寣媴拞偺彫妀桿敪傪挷傋偨丅偦偺寢壥丄12 廡屻偺儔僢僩崪悜偱傕攞悢惈嵶朎偺桿敪偼尒傜傟偢丄6 廡屻偲 12 廡屻偵挷傋偨枛徑愒寣媴偺彫妀偵偮偄偰傕桳堄側憹壛偼擣傔傜傟側偐偭偨 (昞 16)丅
 |
 |
丂埲忋偺寢壥傛傝丄慜弎偺尨巕椡摿掕憤崌尋媶偱幚巤偟偨徠幩僐儉僊偺堚揱撆惈帋尡寢壥偑偡傋偰堿惈偱偁傞帠傕峫椂偟丄崙奜偱曬崘偝傟偰偄傞弶婜偺梲惈寢壥2), 3), 5), 6) 偵偮偄偰偼嵞尰惈偑摼傜傟偢丄徠幩僐儉僊暡偵傛傞堚揱撆惈嶌梡偼側偄傕偺偲峫偊傞丅
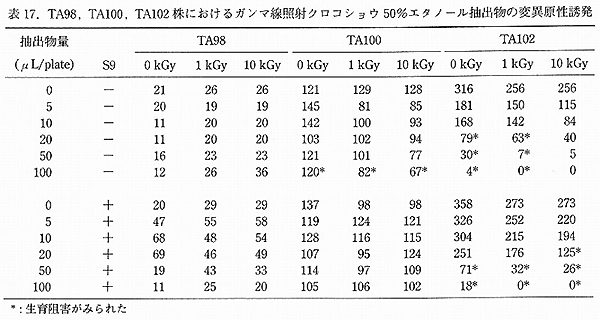
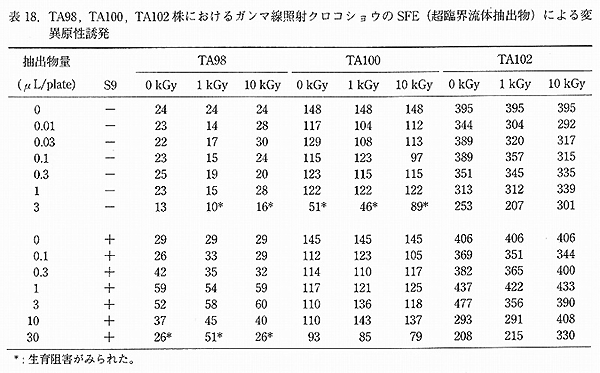
丂崟僐僔儑僂偱偼丄僄僞僲乕儖拪弌暔偲挻椪奅棳懱拪弌偵傛傞拪弌朄偺堘偄偵傛傞曄堎尨惈偺斾妑傪偟偨偲偙傠丄偄偢傟偺拪弌暔偱傕 TA98 偵偍偄偰偺傒戙幱妶惈壔朄偱徠幩丄旕徠幩偲傕偵庛偄曄堎僐儘僯乕悢偺憹壛偑擣傔傜傟偨偑丄徠幩偵傛偭偰憹壛偡傞偙偲偼側偔 乮昞 17乯丄傑偨拪弌朄偵傛傞嵎傕擣傔傜傟側偐偭偨丅愒僩僂僈儔僔偱偼丄旕徠幩偺 TA98 偺戙幱妶惈壔朄偵偍偄偰丄懳徠偺 2 攞掱搙偺曄堎僐儘僯乕悢憹壛偑擣傔傜傟偨偑丄徠幩孮偵偮偄偰偼曄堎僐儘僯乕偺憹壛偼擣傔傜傟側偐偭偨 乮昞 18丄19乯丅僫僣儊僌丄僷僾儕僇偵偮偄偰偼丄徠幩丄旕徠幩偺偄偢傟偺拪弌暔傕慡偰偺梡検偱曄堎僐儘僯乕偺憹壛偼擣傔傜傟側偐偭偨丅崟僐僔儑僂偲愒僩僂僈儔僔偺庛偄曄堎僐儘僯乕桿敪偵偮偄偰偼丄僐僔儑僂偼僐僂僕僇價偑嶻惗偡傞傾僼儔僩僉僔儞偱墭愼偝傟傞帠偑偁傞偙偲偐傜丄崱夞偺拪弌暔偵娭偟偰丄傾僼儔僩僉僔儞偺懚嵼傪敄憌僋儘儅僩僌儔僼傿乕偵傛傝妋擣偟偨偑偦偺懚嵼傪帵偡偙偲偼偱偒側偐偭偨丅偙偺偙偲偐傜丄庛偄曄堎僐儘僯乕偺桿敪偼僐僔儑僂惉暘拞偺暔幙偵傛傞傕偺偲峫偊傜傟偨11)丅
丂僗僷僀僗偼垷擬懷偱惗嶻偝傟傞堊丄旝惗暔傗恀嬠丄媦傃恀嬠偺戙幱嶻暔偱偁傞儅僀僐僩僉僔儞偵傛傞墭愼傪庴偗傗偡偔丄怘昳塹惗忋壗傜偐偺曽朄偵傛傝嶦嬠偡傞昁梫偑偁傞丅偙傟傑偱偦偺旝惗暔墭愼傪寉尭偡傞堊丄廘壔儊僠儖丄EO 僈僗傗抁帪娫偺崅壏嶦嬠偑峴傢傟偰偒偨丅偟偐偟丄廘壔儊僠儖偼撆惈偑嫮偔丄僆僝儞憌攋夡暔幙偱 2005 擭偵偼揚攑偝傟傞梊掕偱偁傝丄堦曽丄EO 僈僗偼嫮偄堚揱撆惈暔幙偱偁傞偙偲偐傜揔愗偲偼偄偊側偄丅崄恏椏偲偟偰偺摿惈傪幐偆偙偲側偔嶦嬠偡傞曽朄偲偟偰丄曻幩慄徠幩偵傛傞嶦嬠偑嵟傕桳岠偲偝傟丄徠幩怘昳偺拞偱傕僗僷僀僗偺徠幩偑懡偔偺崙乆偱嵦梡偝傟偰偄傞丅偟偨偑偭偰丄怘暔偺戝晹暘傪奀奜偐傜偺桝擖偵棅偭偰偄傞傢偑崙偱偼丄変乆偺抦傜側偄偆偪偵怘偟偰偄傞壜擻惈傕斲掕偱偒側偄偙偲偐傜丄専抦朄偵傛傞幆暿傕廳梫偲側傞丅僗僷僀僗偼庬椶傕懡偔丄偦偺傕偺偺惗棟嶌梡偵偮偄偰偼懡偔偺曬崘偑偁傞堦曽偱丄徠幩僗僷僀僗偺埨慡惈偵娭偡傞曬崘偼彮側偄丅杮尋媶偱偼嵶嬠傪梡偄傞暅婣曄堎帋尡偺僨乕僞傪帵偟偨偑丄攟梴嵶朎傗摦暔傪梡偄偨堚揱撆惈帋尡偼枹偩峴傢傟偰偍傜偢丄儕僗僋昡壙偺娤揰偐傜丄奺庬偺帋尡宯偺僨乕僞偑昁梫偲偝傟傞怘昳偱偁傞丅
 |
 |
 |
丂杮崁偱偼丄恅栰尋媶強偱幚巤偟偨徠幩怘昳偺堚揱撆惈偵娭偡傞僨乕僞傪傑偲傔丄栐梾揑偵奣愢偟偨丅搳梌検偲偟偰偼偐側傝夁崜側帋尡忦審偵傕偐偐傢傜偢丄帋尡偟偨徠幩怘昳偺慡偰偵堿惈偺寢壥偑摼傜傟丄栤戣偲側傞傛偆側揰偼傒傜傟側偐偭偨偙偲偐傜丄杮帋尡忦審壓偱偼丄徠幩怘昳偺堚揱撆惈偼側偄傕偺偲峫偊傞丅
丂変乆偑晛抜偐傜怘偟偰偄傞帺慠怘昳傗揤慠揧壛暔偵偍偄偰傕堚揱撆惈傪帵偡怘昳偼悢懡偔偁傞丅嫑傗擏偺從偗徟偘偱抦傜傟傞偛偲偔壛擬挷棟偡傞偙偲偱嫮楏側敪偑傫暔幙偑惗惉偝傟傞偙偲傕暘偐偭偰偒偨偑丄偦偺屻偺尋媶偵傛傝摨帪偵栰嵷椶傪怘傋傞偙偲偱堚揱撆惈嶌梡偑寉尭丒徚幐偡傞帠傗丄変乆帺恎偑偦偺晹暘傪怘傋側偄帠偱偦偺撆嶌梡傪夞旔偡傞傛偆偵側偭偰偒偨丅怘昳徠幩偼怘昳曐懚傗怘昳塹惗偺柺偐傜嬌傔偰岠壥揑偱偁傝丄梡偄傜傟傞幚梡揑側徠幩慄検偱偼丄怘姶偑懝側傢傟偢塰梴惉暘偺曄壔傕彮側偄側偳偺儊儕僢僩偑偁傞偙偲偐傜丄懡偔偺崙偱怘昳偵徠幩偝傟偰偄傞丅堦曽崅慄検偱偼丄僌儖僐乕僗偺傛偆偵摿掕偺塰梴惉暘偺曄壔偵傛偭偰曄堎尨惈暔幙偑惗偠丄偦傟偼傑偨壥幚拞偺惉暘偱晄妶壔偝傟傞椺傕抦傜傟偰偄傞12-16)丅偙偺傛偆偵丄徠幩偵傛偭偰婲偙傝偆傞壜擻惈偺偁傞枹抦偺惉暘曄壔傗惗惉暔偵懳偡傞惗暔嶌梡偵娭偟偰偼丄僶僀僆傾僢僙僀偵傛偭偰徠幩慄検偺撆惈妛揑側埨慡堟傪妋擣偟丄徚旓幰偑埨怱偟偰怘傋傜傟傞傛偆側壢妛揑側僨乕僞傪採嫙偡傞帠偑廳梫偱偁傞丅
丂徠幩怘昳偺寬慡惈 / 埨慡惈昡壙偵偮偄偰憗偔偐傜偦偺廳梫惈傪彞偊傜傟丄杮尋媶偵偛彆尵壓偝偭偨徏嶳峎攷巑偵怺偔姶幱怽偟忋偘傑偡丅側偍杮峞偼丄恅栰尋媶強堚揱撆惈晹栧偺慴傪嶌傜傟偙偺尋媶偺巜婗傪偲傜傟偨 (屘) 娾尨斏梇攷巑偲丄尰嵼偼悢柤偺儊儞僶乕偟偐恅栰尋媶強偵嵼愋偟偰偄側偄偑丄摉帪愭攜摨椈偲偟偰堦弿偵尋媶傪峴偭偨丄廰扟揙攷巑丄崅捁峗夘攷巑丄幒揷揘榊攷巑丄壛摗婎宐攷巑丄嶳塭峃師攷巑丄嶁杮 (峳愳) 嫗巕丄嬥巜 (愳忋) 媣旤巕偺奺巵偵偝偝偘偨偄丅
1) 娾尨斏梇 : 恅栰尋媶強偱幚巤偝傟偨徠幩怘昳偺堚揱撆惈帋尡, 恅栰尋媶強擭曬, 6, 77-88 (1983).
2) Vijayalaxmi and G. Sadasivan : Int. J. Radiat. Biol., 27, 135-142 (1975).
3) Vijayalaxmi and S. G. Srikantia : India. Radiat. Phys. Chem., 34, 941-952 (1989).
4) V. A. Kopylov et al. : Radiobilogia, 12, 524 (1972).
5) H. W. Renner : Toxicology, 8, 213-222 (1977).
6) C. Bhaskaram and G. Sadasivan : Am. J. Clin. Nutr., 28, 130-135 (1975).
7) 椦 恀 : 乽彫妀帋尡乿亅幚尡朄偐傜僨乕僞偺昡壙傑偱亅, 僒僀僄儞僥傿僗僩幮 (1991).
8) H. V. Levinsky and M. A. Wilson : Food Cosmet. Toxicol., 13, 243 (1975).
9) J. M. Tesh et al. : Studies in rats fed a diet incorporating irradiated wheat, International project in the field of food irradiation, pp.1-64, Techinical report series IFIP-R 45, October (1977).
10) 揷拞寷曚 : 徠幩僐儉僊暡帞椏媼塧偵傛傞僠儍僀僯乕僘丒僴儉僗僞乕偍傛傃儔僢僩崪悜嵶朎偵抲偗傞攞悢惈嵶朎偺桿敪偲枛徑愒寣媴拞偺彫妀桿敪, 怘昳徠幩埾堳夛丒尋媶惉壥嵟廔曬崘彂, 擔杮傾僀僜僩乕僾嫤夛, 212-219 (1992).
11) 嶁杮嫗巕 : 僈儞儅慄徠幩僗僷僀僗丒儅儞僑乕偺曄堎尨惈, 怘昳徠幩埾堳夛丒尋媶惉壥嵟廔曬崘彂, 擔杮傾僀僜僩乕僾嫤夛, 205-211 (1992).
12) 愳娸弚楴 : 僈儞儅慄徠幩摐塼偺曄堎尨惈偍傛傃偦偺梷惂, 怘昳徠幩埾堳夛丒尋媶惉壥拞娫曬崘彂, 擔杮傾僀僜僩乕僾嫤夛, 119-130 (1989).
13) 慶晝擈弐梇, 愇娰婎 : 徠幩僌儖僐乕僗偺僠儍僀僯乕僘丒僴儉僗僞乕嵶朎偵傛傞愼怓懱堎忢帋尡, 怘昳徠幩埾堳夛丒尋媶惉壥拞娫曬崘彂, 擔杮傾僀僜僩乕僾嫤夛, 131-146 (1989).
14) 嶁杮嫗巕, 娾尨斏梇 : 徠幩怘昳偍傛傃徠幩僌儖僐乕僗偺僒儖儌僱儔傪梡偄傞曄堎尨惈帋尡, 怘昳徠幩埾堳夛丒尋媶惉壥拞娫曬崘彂, 擔杮傾僀僜僩乕僾嫤夛, 147-162 (1989).
15) 慶晝擈弐梇, 愇娰婎 : 僈儞儅慄徠幩僌儖僐乕僗偵偮偄偰偺曄堎尨惈帋尡, 怘昳徠幩埾堳夛丒尋媶惉壥嵟廔曬崘彂, 擔杮傾僀僜僩乕僾嫤夛, 150-181 (1992).
16) 嶁杮嫗巕, 娾尨斏梇 : 僈儞儅慄徠幩僌儖僐乕僗偺曄堎尨惈, 怘昳徠幩埾堳夛丒尋媶惉壥嵟廔曬崘彂, 擔杮傾僀僜僩乕僾嫤夛, 182-191 (1992).
乮2004 擭 8 寧 9 擔庴棟乯
|
|