俥倝倗丏侾丏 俙倫倫倎倰倎倲倳倱丂倖倧倰丂倣倕倎倱倳倰倕倣倕値倲丂倧倖丂俤倛丂倝値丂倖倝倱倛丂倛倧倣倧倗倕値倎倲倕倱丏
 |
丂堦斒偵嫑偺曻幩慄徠幩偵傛傞曐憼偵偍偄偰偼丄掅慄検儗儀儖乮侽丏侾乣侽丏俆俵倰倎倓乯偺曻幩慄僷僗僣儕僛乕僔儑儞偑桳棙偲偝傟偰偄傞丅偟偐偟側偑傜丄偦偺傛偆傗掅慄検徠幩偱偼丄堦斒晠攕嵶嬠偺傎偲傫偳偼巰柵偡傞偱偁傠偆偑丄儃僣儕僰僗俤宆嬠夎朎偼偦偺俢抣乲俁丆俈丆俋乴偐傜傒偰丄偐側傝偺悢偑惗偒巆傝丄偦偺寢壥敪堢偵岲揔忦審偑梌偊傜傟傞側傜偽丄偄偮偱傕撆慺傪嶻惗偡傞壜擻惈偑偁傞偱偁傠偆丅
丂俽們倛倣倝倓倲傜乲俉乴偼曻幩慄徠幩偵偍偗傞僷僗僣儕僛乕僔儑儞慄検偼丄儃僣儕僰僗俤宆嬠夎朎傪姰慡偵嶦柵偟摼側偄偱偁傠偆偲弎傋偰偄傞丅傑偨俠倎値値傜乲係丆俆乴偼嫑偵偍偗傞儃僣儕僰僗俤宆嬠偺愙庬帋尡偵偍偄偰丄徠幩偵惗偒巆偭偨俤宆嬠夎朎偑丄偙傟偵憡摉偡傞悢偺徠幩偝傟側偄嫑偵偍偗傞夎朎傛傝傕偭偲懍偔敪堢偟偰撆慺傪嶻惗偡傞偙偲傪擣傔丄曻幩慄僷僗僣儕僛乕僔儑儞偟偨嫑偑儃僣儕僰僗俤宆嬠偵傛偭偰懍偐偵撆惈壔偝傟傞壜擻惈傪埫帵偟偨丅
丂偙偺傛偆偵嫑偺曻幩慄僷僗僣儕僛乕僔儑儞偵娭偟偰偼丄儃僣儕僰僗俤宆嬠偵懳偡傞埨慡惈偺揰偱側偍媈栤偺梋抧偑巆偝傟偰偄傞丅偦偙偱崱夞偺傢傟傢傟偺幚尡偵偍偄偰偼丄俤宆嬠夎朎傪愙庬偟偨嫑擏儂儌僕僃僱乕僩傪梡偄丄偙傟傪掅慄検徠幩偟偨屻幒壏晬嬤乮俀侽亷丆侾侽亷乯偵曐懚偟偨応崌丄撆慺嶻惗偑偳偺傛偆偵偟偰婲傞偐傪丄晠攕偲偺娭楢惈偁傞偄偼巁壔娨尦揹埵偺曄壔側偳偐傜捛媶偡傞偙偲偲偟偨丅
丂怴慛側僯僔儞偺擏幙晹偵偙傟偲摨検偺柵嬠忲棴悈傪壛偊偰儈僉僒乕偵偐偗丄儂儌僕僃僱乕僩傪嶌惢偟偨丅偙傟傪帋尡娗乮侾俉亊侾俆侽倣倣乯偵奺侾侽倗偢偮暘拲偟丄偝傜偵俠倢倧倱倲倰倝倓倝倳倣丂倐倧倲倳倢倝値倳倣丂倲倷倫倕丂俤丂俬倵倎値倎倝敪朎傪丄侾侽丒俤乮俆乯乛倗偺妱偵愙庬偟偨丅愙庬偝傟偨帋尡娗偼徠幩偡傞傑偱昘椻壓偵曐懚偟偨丅
丂愙庬偝傟偨帋尡偼丄梻挬僐僶儖僩俇侽乮栺侾丆俉侽侽俠倝乯徠幩憰抲偱侽丏侾偍傛傃侽丏俁俵倰倎倓偺徠幩検偱徠幩偝傟偨丅徠幩拞偺壏搙偼侾侽乣係亷傪曐偭偨丅徠幩捈屻椉慄検嬫暘偲傕旕徠幩僐儞僩儘乕儖偲偲傕偵偦傟偧傟侾侽亷傑偨偼俀侽亷偺峆壏婍偵擖傟偰曐懚偟偨丅
丂堦掕婜娫曐懚偟偨帋尡娗傪偲傝弌偟丄偦偺撪梕暔傪暿偺柵嬠梕婍偵俀侽倣倢偺侽丏侾亾儁僾僩儞惗棟怘墫悈梟塼偱姰慡偵愻偄弌偡丅偙傟傪傛偔崿崌偟偰埲壓偺帋尡偵嫙偟偨丅
丂忋婰帋椏傪俀丆侽侽侽倰倫倣丆侾俆暘娫墦怱暘棧偟偰偦偺忋惔傪偲傝丄偙傟偵摨検偺侽丏俀亾僩儕僾僔儞乮侾丗俀俆侽乯儕儞巁僶僢僴乕乮倫俫俇丏侽乯梟塼傪壛偊偰俁俈亷偵侾帪娫僀儞僉儏儀乕僩偡傞丅妶惈壔偝傟偨撆慺塼傪僛儔僠儞儕儞巁僶僢僴乕乮倫俫俇丏侽乯偱婓庍偟丄偦偺侽丏俆倣倢傪奺俀旵偢偮偺儅僂僗暊峯撪偵拲幩偟偨丅揟宆揑儃僣儕僰僗拞撆徢忬傪掓偟偰巰朣偡傞傑偱俀擔娫娤嶡偟偨丅
丂俠倧倰倢倕倲倲傜乲俇乴偺俿俹俶姦揤傪梡偄偰擇廳暯斅朄傪峴側偭偨丅俀俆亷偱係俉帪娫攟梴偟偰慡僐儘僯乕悢傪僇僂儞僩偟偨丅
丂俠倧値倵倎倷偵旝検奼嶶暘愅朄偵傛偭偨丅
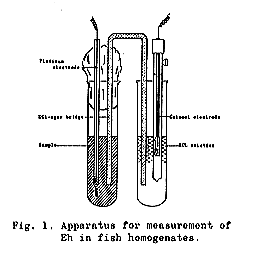
丂徠幩偍傛傃旕徠幩帒椏偺俤倛傪應掕偡傞憰抲傪俥倝倗丏侾偵帵偡丅敀嬥揹嬌偼僋儘儉棸巁偵偮偗偰傛偔惔忩偵偟丄忲棷悈偱姰慡偵愻偭偨屻丄巊梡捈慜偵儊僞僲乕儖墛偱姡憞偟偨丅揹嬌傪儂儌僕僃僱乕僩偡傞応崌丄偱偒傞偩偗怺偔捑傔偨丅俤倛偺應掕偼乽擔棫亅杧応乿俵亅俆宆倫俫儊乕僞乕偵帺摦婰榐憰抲傪偮偗偰峴側偭偨丅應掕拞帋椏亅揹嬌宯傪側傞傋偔棎偝側偄傛偆偵拲堄偟偨丅
 |
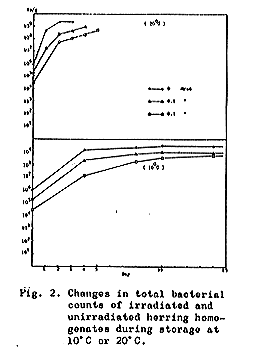
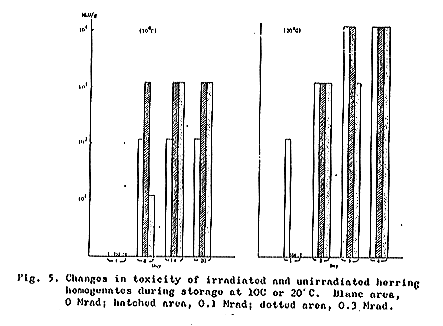
丂嬠悢偺曄壔傪俥倝倗丏俀偵帵偡丅侽丏侾偍傛傃侽丏俁俵倰倎倓偺徠幩偼丄嵟弶偺嬠悢傪偦傟偧傟俉俀丏侽亾偍傛傃俋俈丏俀亾偵尭彮偝偣偨丅俀侽亷曐懚偺応崌丄旕徠幩帋椏偺嬠悢偼媫懍偵憹壛偟偰俀擔屻偵嵟崅抣偵払偟偨偑丄徠幩帋椏偺偦傟偼傕偭偲備偭偔傝偱俆擔屻偵嵟崅抣偵払偟偨丅堦曽侾侽亷曐懚偺応崌丄俀侽亷曐懚偲傎乁摨條偺孹岦偑傒傜傟偨偑丄徠幩偍傛傃旕徠幩帋椏偺偍偺偍偺偑偦偺嵟崅抣偵払偡傞偺偵丄俀侽亷偺応崌偺栺係攞偺擔悢傪梫偟偨丅
 |
丂俥倝倗丏俁偵帵偡傛偆偵丄旕徠幩帋椏偱偼椉曐懚壏搙偲傕傎偲傫偳捈慄揑憹壛偑傒傜傟偨丅堦曽徠幩帋椏偱偼偄偔暘儔僌偑傒傜傟丄偦偺屻備偭偔傝憹壛傪帵偟偨丅
丂俿倁俛偑俁侽倣倗亾傪挻偊傞偲丄柧傜偐偵晠攕廘偑慡帋椏偵偮偄偰擣傔傜傟偨丅徠幩偍傛傃旕徠帋椏偺俿倁俛偑俁侽倣倗亾傪挻偊傞嵺偺曐懚擔悢偼丄旕徠幩帋椏偱偼丄侾侽亷偱俀乣係擔丄俀侽亷偱侾擔偱偁傝丄侽丏侾俵倰倎倓徠幩帋椏偱偼丄侾侽亷偱俉乣侾侽擔丄俀侽亷偱俁擔偱偁傝丄傑偨侽丏俁俵倰倎倓徠幩帋椏偱偼丄侾侽亷偱侾俀乣侾係擔丄俀侽亷偱俆擔偱偁偭偨丅
 |
丂曐懚婜娫拞偺俤倛偺曄壔傪丄揹埵帪娫嬋慄偲偟偰捛愓偡傞偲俥倝倗丏係偵帵偡偲偍傝偱偁傞丅
丂旕徠幩帋椏傪侾侽亷偵曐懚偟偨応崌丄揹埵偼弶傔亅侽丏侽俁儃儖僩偐傜彊乆偵掅壓偟丄俇擔屻偵嵟掅抣偵亅侽丏俁俁儃儖僩偵側傝丄偦傟偐傜備偭偔傝忋徃偟偰侾俆擔屻偵偼亅侽丏俀侽儃儖僩傪帵偟偰偄偨丅摨帋椏傪俀侽亷偵曐懚偟偨応崌偼丄揹埵偼媫懍偵掅壓偟丄俁俇帪娫偱嵟掅抣亅侽丏俁俆儃儖僩偵払偟丄師偄偱廔嬊揹埵偺亅侽丏俀侽儃儖僩偵傑偱忋徃偟偨丅
丂堦曽徠幩帋椏偱偼丄尠挊側偙偲偵丄偡傋偰偺弶婜揹埵偼旕徠幩帋椏偺偦傟傛傝偝傜偵儅僀僫僗懁偵娚徴偝傟偰偄偨丅侾侽亷曐懚偺応崌丄弶婜揹埵偼侽丏侾偍傛傃侽丏俁俵倰倎倓偱偦傟偧傟亅侽丏俀俆偍傛傃亅侽丏俁係儃儖僩偱偁偭偨丅偙傟傜偺揹埵偼曐懚婜娫拞偄偔傜偐攇偺偁傞曄摦傪宱偰丄侽丏侾偍傛傃侽丏俁俵倰倎倓偱偦傟偧傟亅侽丏俀侽偍傛傃亅侽丏俁侾儃儖僩偺廔嬊揹埵傪帵偟偨丅傑偨俀侽亷曐懚偺応崌丄弶婜揹埵偼侽丏侾偍傛傃侽丏俁俵倰倎倓偱偦傟偧傟亅侽丏侾俋偍傛傃亅侽丏俀俈儃儖僩傪帵偟丄廔嬊揹埵偼摨偠偔侽丏侾侾儃儖僩傪帵偟偨丅
 |
丂徠幩偍傛傃旕徠幩帋椏偺侾侽亷偍傛傃俀侽亷曐懚拞偵偍偗傞撆慺嶻惗偺曄壔傪帵偡偲丄俥倝倗丏俆偺偲偍傝偱偁傞丅
丂侾侽亷曐懚偺応崌丄偡傋偰偺帋椏偵偮偄偰係擔屻偵専弌偟摼傞検偺撆慺偼尒弌偝傟側偐偭偨丅偟偐偟俉擔屻偱偼懡偐傟彮側偐傟撆慺偑専弌偝傟偨丅侽丏侾俵倰倎倓徠幩帋椏偵嵟崅儗儀儖偺撆慺偑尒弌偝傟偨偑丄侽丏俁俵倰倎倓偺傕偺偼嵟掅偱偁偭偨丅侾係亅俀侽擔娫偺曐懚偱偼丄旕徠幩帋椏傛傝傕偭偲懡偔偺撆慺偑椉徠幩検偺帋椏拞偵尒弌偝傟偨丅
丂俀侽亷曐懚偺応崌丄旕徠幩帋椏偱偼傢偢偐侾擔屻偵撆惈偑擣傔傜傟傞傛偆偵側傝丄俁擔屻偵偼嵟崅偺嫮偝偵払偟偨丅堦曽徠幩帋椏偱偼俀擔屻偵撆惈傪帵偡傛偆偵側傝丄侽丏侾俵倰倎倓偱偼俁擔屻丄侽丏俁俵倰倎倓偱偼係擔屻偵偦傟偧傟嵟崅抣傪帵偟偨丅
丂撆慺嶻惗偼侾侽亷傛傝俀侽亷曐懚偺曽偑丄偦偺惗惉懍搙偍傛傃嫮偝偺揰偱桪傟偰偄傞偙偲偑傢偐傞丅
 |
丂慡嬠悢偺曄壔傪俿倁俛偍傛傃俤倛偺曄壔偲斾妑偡傞偲丄徠幩帋椏偵偍偗傞偙傟傜偺曄壔抣娫偺娭學偼丄旕徠幩帋椏偵偍偗傞偦傟偲傗傗堎側偭偰偄傞丅偡側傢偪旕徠幩帋椏偱偼丄嬠悢偼俿倁俛偺捈慄揑憹壛偍傛傃俤倛偺弶婜偺掅壓偲暯峴偟偰偄傞偑丄徠幩帋椏偱偼丄偙傟傜偺抣偺曄壔偼昁偢偟傕暯峴偟偰偄側偄丅徠幩帋椏偺俿倁俛偺惗惉懍搙偼斾妑揑抶偔丄廬偭偰嬠悢偑侾侽丒俤乮俈乯偺僆乕僟乕傪挻偊傞傑偱俿倁俛偺捈慄揑憹壛偼傒傜傟側偐偭偨丅偟偐傕揹埵帪娫嬋慄偵偙傟傜偺曄壔偼斀塮偝傟偰偄側偄丅偦偺尨場偼丄婗敪惈墫婎偺敪惗偵桼棃偡傞旝惗暔偑徠幩偵傛偭偰偄偪偠傞偟偔尭彮偟偨偨傔偲峫偊傜傟傞丅
丂愭偵挊幰傜乲俀乴偼崅埑柵嬠偟偨嫑擏儂儌僕僃僱乕僩偑丄偦偺掅偄弶婜揹埵偺偨傔儃僣儕僰僗俤宆嬠偺敪堢偵偲偭偰奿岲偺攟抧偵側傞摼傞偙偲丄偦偟偰傑偨柵嬠偟側偄嫑擏偱傕曐懚拞偵婲傞晠攕偁傞偄偼帺屓徚壔偵偲傕側偆俤倛偺媫寖側掅壓偺偨傔丄摨嬠偺敪堢偲撆慺嶻惗傪傕偨傜偡偙偲傪曬崘偟偨丅
丂崱夞偺幚尡偵偍偄偰丄巁壔娨尦揹埵偺應掕偵娭偟偰丄偲偔偵師偺俀揰偵娭怱偑婑偣傜傟傞丅偡側傢偪丄
丂侾乯曻幩慄僷僗僣儕僛乕僔儑儞慄検偑丄嫑擏偵懳偟偰岲婥惈偐寵婥惈偐偄偢傟偺忦審傪傕偨傜偡偐丅
丂俀乯徠幩偝傟偨嫑擏偺巁壔娨尦揹埵偺應掕偑丄儃僣儕僰僗俤宆嬠偺敪堢傪敾抐偡傞堦偮偺巜昗偵側傝摼傞偐丅
丂傢傟傢傟偺梊旛揑幚尡偵傛傞偲丄曻幩慄徠幩偼偁傞岲婥揑攟梴婎偍傛傃嫑擏儂儌僕僃僱乕僩偺拞偺俤倛傪媫寖偵掅壓偝傟摼傞偙偲偑傢偐偭偨丅偨偲偊偽俿俹俧攟抧傪侽丏俁俵倰倎倓徠幩偡傞偲丄俥倝倗丏俇偵帵偡傛偆偵丄俤倛偼亄侽丏侾侾儃儖僩傛傝媫寖偵掅壓偟偰亅侽丏俀俆儃儖僩傪帵偟偨丅偟偐傕徠幩偵傛偭偰偮偔傜傟傞偙偺傛偆側娨尦揑忦審偼丄儃僣儕僰僗俤宆嬠偺敪堢傪巟帩偡傞偙偲偑傢偐偭偨丅偡側傢偪僠僆僌儕僐儗乕僩傪壛偊側偄俿俹俧攟抧偵俤宆嬠夎朎傪愙庬偟偨屻丄侽丏俁俵倰倎倓偵徠幩偟丄師偄偱俀侽亷偱攟梴偡傞偲係俉帪娫埲撪偵柧傜偐偵敪堢偑傒傜傟偨偑丄偙傟偵斀偟偰徠幩偟側偄懳徠偱偼敪堢偑傒傜傟側偐偭偨丅
丂徠幩拞偵偍偗傞俀丆俁偺嫑擏儂儌僕僃僱乕僩偺俤倛偺曄壔傪偟傜傋偨寢壥偼丄俥倝倗丏俈偵帵偝傟偰偄傞丅傢傟傢傟偺崱夞偺幚尡偐傜柧傜偐側傛偆偵丄侽丏侾傑偨偼侽丏俁俵倰倎倓偱徠幩偝傟偨僯僔儞偺儂儌僕僃僱乕僩偼丄偐側傝掅偄儅僀僫僗偺弶婜揹埵傪帵偟偰偍傝丄偦偺偨傔徠幩偵惗偒巆偭偨儃僣儕僰僗俤宆嬠夎朎偺敪堢偲撆慺嶻惗傪巟帩偟偨傕偺偲偄偊傛偆丅
丂堦曽旕徠幩帋椏偵偍偄偰傕摨條偵俤倛偺掅壓偑傒傜傟丄偦偺寢壥俤宆嬠偺敪堢偲撆慺嶻惗偑擣傔傜傟偨丅偙偺応崌偼忋弎偺応崌偲堎側傝丄庡偲偟偰嫑偵晬拝偟偰偄傞岲婥惈儈僋儘僼儘乕儔偺斏怋偵偲傕側偆巁慺徚旓嶌梡偵傛傞傕偺偲峫偊傜傟傞丅
丂徠幩偝傟偨嫑擏偵偍偗傞儃僣儕僰僗俤宆嬠偺敪堢偲撆慺嶻弌偵媦傏偡場巕偲偟偰丄愙庬嬠悢丄徠幩検丄曐懚壏搙偍傛傃婜娫側偳偑戝偄偵娭學偡傞傕偺偲巚傢傟傞丅俙倐倰倎倛倎倣倱倱倧値傜乲侾乴偼僯僔儞僼傿儗乕偵儃僣儕僰僗俤宆嬠夎朎傪俀亊侾侽丒俤乮俇乯乛俇侽倗偺妱偵愙庬偟偨屻丄侽丏俁俵倰倎倓偵徠幩偟偰曐懚偡傞偲丄俀侽亷偱俇係帪娫埲撪偵撆慺偑擣傔傜傟丄偦偟偰恀嬻曪憰偟偨傕偺偺曽偑偟側偄傕偺傛傝偼傞偐偵撆慺擹搙偑崅偐偭偨偲曬崘偟偰偄傞丅俠倎値値傜乲係丆俆乴偼恀嬻曪憰偟偨嫑擏傪徠幩偟偨屻曐懚偟偰撆慺嶻惗傪偟傜傋偨寢壥丄俤宆嬠夎朎傪侾侽丒俤乮俆乯乛侾侽侽倗偺妱偵愙庬偟偰徠幩偝傟偨帋椏偺曽偑丄巆懚悢偵憡摉偡傞夎朎傪愙庬偟偰徠幩偝傟側偐偭偨帋椏傛傝傕懡偔偺撆慺偑専弌偝傟丄偟偐傕偦偺惗惉懍搙傕栺俀攞偱偁偭偨偲弎傋偰偄傞丅偙傟偲摨條偺寢壥偼丄崱夞偺傢傟傢傟偺幚尡寢壥偵偍偄偰傕擣傔傜傟丄徠幩帋椏偺曽偑曻幩慄嶦嬠偵傛偭偰夎朎悢偑尭彮偟偰偄傞偵傕偐偐傢傜偢丄旕徠幩帋椏拞傛傝崅偄擹搙偺撆慺偑専弌偝傟偨丅偙傟傜偺娤嶡傪婎偵偡傟偽丄曻幩慄僷僗僣儕僛乕僔儑儞偼丄僯僔儞擏偵偍偗傞儃僣儕僰僗俤宆嬠偺撆慺嶻惗傪丄偁傞忦審偱偼彆挿偡傞偐偺傛偆偵傒偊傞丅偦偺尨場偲偟偰偼丄忋弎偺傛偆偵徠幩拞偵偍偙傞巁壔娨尦揹埵偺掅壓偑俤宆嬠偺敪堢偵桳棙側忦審傪梌偊傞偨傔偲峫偊傜傟傞丅
丂杮尋媶偼俬俙俤俙埾戸尋媶旓乮No俁侾俆侾俼俛乯偺曗彆偵傛傝峴側傢傟偨傕偺偱偁傞丅
 |
 |
丂僯僔儞偺儂儌僕僃僱乕僩偵儃僣儕僰僗俤宆嬠夎朎傪侾侽丒俤乮俆乯乛倗偺妱偵愙庬偟偰侽丆侽丏侾丆侽丏俁俵倰倎倓偵徠幩偟偨屻丄俀侽亷傑偨偼侾侽亷偵曐懚偟偨丅曐懚拞堦斒嵶嬠悢丄婗敪惈墫婎丄撆惈丄偍傛傃巁壔娨尦揹埵摍偑應掕偝傟丄偙傟傜偺巜帵抣娫偺曄壔傪徠幩帋椏偲旕徠幩帋椏偲偺娫偱斾妑偟偨丅
丂旕徠幩帋椏偵偍偗傞撆慺嶻惗偼旕忢偵懍偄偺偱丄撆慺嶻惗偵梫偡傞帪娫偲晠攕帪娫偲偺娫偵嵎偑傒傜傟側偄丅堦曽徠幩帋椏偵偍偗傞撆慺嶻惗偼丄晠攕偺擣傔傜傟傞慜偵婲傝巒傔傞偙偲偑傢偐偭偨丅偟偐傕徠幩帋椏偺曽偑旕徠幩帋椏傛傝懡偔偺撆慺偑専弌偝傟偨丅
丂曻幩慄僷僗僣儕僛乕僔儑儞偑丄僯僔儞嫑擏偵偍偗傞儃僣儕僰僗俤宆嬠偺敪堢偲撆慺嶻惗傪彆挿偡傞偐偺傛偆側帠幚傪丄嫑擏偵偍偗傞巁壔娨尦揹埵偺棫応傛傝榑偠偨丅
乲侾乴俙倐倰倎倛倎倣倱倱倧値丆俲丏丆俢倕丂俽倝倢倴倎丆俶丏俶丏丆
丂丂丂倎値倓丂俵倧倢倝値丆俶丏
丂丂丂丗俠倎値倎倓丏俰丏俵倝們倰倧倐倝倧倢丏丆侾侾丆
丂丂丂俆俀俁亅俆俀俋乮侾俋俇俆乯
乲俀乴埨摗朏柧丄堜忋彑峅丗擔杮悈嶻妛夛帍丄俀俁丆係俆俉亅係俇俀
丂丂丂乮侾俋俆俈乯
乲俁乴埨摗朏柧丄幁搰揷棽丄彫栰掝擇丄斞揷峀晇丗杮帍丄戞俁姫丄戞侾崋丆
丂丂丂俆乣侾俀乮侾俋俇俋乯
乲係乴俠倎値値丆俢丏俠丏丆倂倝倢倱倧値丆俛丏俛丏丆俫倧倐倐倱丆俧丏丆
丂丂丂倎値倓丂俽倛倕倵倎値丆俰丏俵丏丗俰丏俙倫倫倢丏俛倎們倲丏丆
丂丂丂俀俉丆係俁侾亅係俁俇乮侾俋俇俆乯
乲俆乴俠倎値値丆俢丏俠丏丆倂倝倢倱倧値丆俛丏俛丏丆
丂丂丂俽倛倵倕倎値丆俰丏俵丏丆俼倧倐倕倰倲倱丆俿丏俙丏丆
丂丂丂倎値倓丂俼倛倧倓倕倱丆俢丏俶丏丗俰丏俙倫倫倢丏俛倎們倲丏丆
丂丂丂俀俋丆俆係侽亅俆係俉乮侾俋俇俇乯
乲俇乴俠倧倰倢倕倲倲丆俰倰丏俢丏俙丏丆俴倕倕丆俰丏俽丏丆
丂丂丂倎値倓丂俽倝値値倛倳倐倧倰丆俼丏俷
丂丂丂丗俙倫倫倢丏俵倝們倰倧倐倝倧倢丏丆侾俁丆俉侽俉亅俉侾俈
丂丂丂乮侾俋俇俆乯
乲俈乴俼倧倐倕倰倲倱丆俿丏俙丏倎値倓丂俬値倗倰倎倣丆俵丏
丂丂丂丗俰丏俙倫倫倢丏俛倎們倲丏丆俀俉丆侾俀俆亅侾係侾乮侾俋俇俆乯
乲俉乴俽們倛倣倝倓倲丆俠丏俥丏丆俴倕們倛倧倵倝們倛丆俼丏倁丏丆
丂丂丂倎値倓丂俥倧倢倝値倎倸倸倧丆俰丏俥丏丗俰丏俥倧倧倓丂俽們倝丏丆
丂丂丂俀俇亅俇俀俇亅俇俁侽乮侾俋俇侾乯
乲俋乴俽們倛倣倝倓倲丆俠丏俥丏丆俶倎値倠丆倂丏俲丏丆
丂丂丂倎値倓丂俴倕們倛倧倵倝們倛丆俼丏倁丏丗俰丏俥倧倧倓丂俽們倝丏丆
丂丂丂俀俈丆俈俈亅俉係乮侾俋俇俀乯
|
|